题目内容
10.以下实验中不能够获得成功的是( )| A. | 将乙烷和氯气的混合气放在光照条件下反应制备氯乙烷(C2H5Cl) | |
| B. | 将乙醇迅速加热至170度制乙烯 | |
| C. | 将还原铁粉、液溴和苯混合制溴苯 | |
| D. | 用电石粉末和水反应制取乙炔 |
分析 A.光照下的取代反应为链锁反应;
B.乙醇发生消去反应生成乙烯;
C.苯与液溴发生取代反应生成溴苯;
D.碳化钙与水反应生成乙炔.
解答 解:A.光照下的取代反应为链锁反应,不能制备纯净的氯乙烷,故A错误;
B.乙醇发生消去反应生成乙烯,迅速加热至170℃,防止生成乙醚,故B正确;
C.苯与液溴发生取代反应生成溴苯,Fe与溴反应生成溴化铁作催化剂,故C正确;
D.碳化钙与水反应生成乙炔,粉末的接触面积大,反应较快,故D错误;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、制备实验是解本题关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
1.高岭土中中SiO2的质量分数为( )
| A. | 46.5% | B. | 23.3% | C. | 21.7% | D. | 35.7% |
5.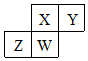 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
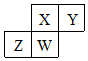 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Y、Z、W的最高化合价分别与其主族序数相等 | |
| C. | 最简单气态氢化物的热稳定性:X>Z>W | |
| D. | 最高价氧化物对应水化物的酸性:X>Z>W |
15.下列说法不正确的是( )
| A. | Cl2、Br2、I2的分子间作用力依次减小 | |
| B. | 石英是由硅原子和氧原子构成的原子晶体,加热熔化时需破坏共价键 | |
| C. | 氢氧化钠在熔融状态下离子键被削弱,形成自由移动的离子,具有导电性 | |
| D. | 水电解生成氢气和氧气,有化学键的断裂和形成 |
2.气态烃1体积可与2体积氯化氢发生加成,生成氯代烷烃,此氯代烷烃1mol可与6mol氯气发生完全的取代反应,则该烃的结构简式为( )
| A. | CH2=CH2 | B. | CH2=CHCH=CH2 | C. | CH4 | D. | CH≡C-CH3 |
19.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | FeCl2溶液:K+、Na+、SO42-、AlO2- | |
| B. | 使紫色石蕊试液变红的溶液:Na+、Fe2+、NO3-、SO42- | |
| C. | 向存在大量Na+、Cl-的溶液中通入足量的NH3后:NH4+、Fe3+、SO42- | |
| D. | 在强酸性溶液中:K+、Fe2+、SO42-、Br- |
20.下列离子方程式书写正确的是( )
| A. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉:Fe3++Fe═2Fe3+ | |
| D. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
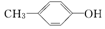 ;③C2H5OH;④CH3CH2Br;⑤CCl4;⑥CH3COOCH3;⑦CH3COOC2H5.据官能团的不同可分为( )
;③C2H5OH;④CH3CH2Br;⑤CCl4;⑥CH3COOCH3;⑦CH3COOC2H5.据官能团的不同可分为( )