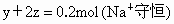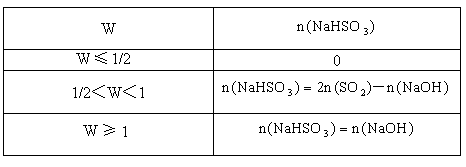题目内容
接触法制硫酸排放的尾气中,含少量的二氧化硫.为防止污染大气,在排放前设法进行综合利用.
(1)某硫酸厂每天排放的10000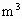 尾气中含0.2%(体积分数)的
尾气中含0.2%(体积分数)的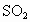 .问用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克石膏
.问用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克石膏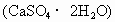
(2)如果将一定体积的尾气通入100mL2mol/L的氢氧化钠溶液使其完全反应,经测定所得溶液含16.7g溶质.试分析该溶液的成分,并计算确定各成分的物质的量.
(3)工厂在尾气处理制石膏的过程中,中间产物是亚硫酸氢钠.调节尾气排放的流量,以取得二氧化硫与氢氧化钠间物质的量的最佳比值,从而提高亚硫酸氢钠的产量.现设n(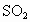 )、n(NaOH)、n(
)、n(NaOH)、n( )分别表示二氧化硫、氢氧化钠和亚硫酸氢钠的物质的量.
)分别表示二氧化硫、氢氧化钠和亚硫酸氢钠的物质的量.
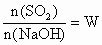 ,试写出W在不同取值范围时,n(
,试写出W在不同取值范围时,n( )的值或n(
)的值或n( )与n(
)与n(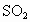 )、n(NaOH)间的关系式.
)、n(NaOH)间的关系式.

解析:
|
(1) 由硫原子守恒可得关系式:
(2) 要运用极端假设法进行推断,溶液中可能发生两个反应:① 设混合物中
解之得: 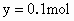 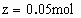
接下来是分区间讨论计算:得结果: (3)
本题较好地体现了高考的要求,侧重考查综合运用能力,设计颇具特色:计算与推断相结合;数学与化学的综合应用;化学知识与环保相互联系.因此反映了高考化学计算命题的发展趋势和特点. |

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
Ⅰ | 7.4 | 40.00 | 1.68 |
Ⅱ | 14.8 | 40.00 | 3.36 |
Ⅲ | 22.2 | 40.00 | 1.12 |
Ⅳ | 37.0 | 40.00 | 0.00 |
(1)实验过程中有关反应的离子方程式为:________________________________。
(2)由Ⅰ组数据直接推测:标准状况下用3.7 g样品进行同样实验时,生成氨气的体积为________L。
(3)试计算该混合物中的(NH4)2SO4和NH4HSO4物质的量之比________。
(4)欲计算该NaOH溶液的物质的量浓度,应选择第________组数据,由此求得NaOH溶液的物质的量浓度为________。
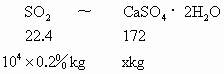
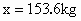
 :
: :
: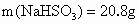 .今
.今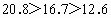 ,所以该溶液成分为
,所以该溶液成分为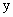 ,
,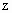
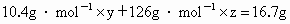 (质量守恒)
(质量守恒)