题目内容
研究化学反应原理对于生产生活是很有意义的.
(1)请设计一个实验装置,使铜与稀硫酸反应生成硫酸铜与氢气.在下面的方框内画出装置图,并标明电极材料名称和电解质溶液名称.

(2)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图1所示:
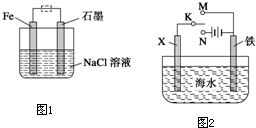
①写出石墨电极的电极反应式: .
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改 .
③写出修改后石墨电极的电极反应式: .
(3)利用如图2装置,可以模拟铁的电化学防护.若X为锌,开关K置于M处,该电化学防护法称为 .
(1)请设计一个实验装置,使铜与稀硫酸反应生成硫酸铜与氢气.在下面的方框内画出装置图,并标明电极材料名称和电解质溶液名称.

(2)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图1所示:

①写出石墨电极的电极反应式:
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改
③写出修改后石墨电极的电极反应式:
(3)利用如图2装置,可以模拟铁的电化学防护.若X为锌,开关K置于M处,该电化学防护法称为
分析:(1)使铜与稀硫酸反应生成硫酸铜与氢气,应设计成电解池,铜为阳极,电解质溶液为硫酸,阴极可为碳;
(2)①发生吸氧腐蚀,石墨为正极,氧气得电子被还原生成OH-;
②成为钢铁电化学防护的装置,铁连接电源的负极;
③形成电解池反应,石墨为阳极,氯离子被氧化生成氯气;
(3)若X为锌,开关K置于M处,锌为负极,被氧化,铁为正极,发生还原反应.
(2)①发生吸氧腐蚀,石墨为正极,氧气得电子被还原生成OH-;
②成为钢铁电化学防护的装置,铁连接电源的负极;
③形成电解池反应,石墨为阳极,氯离子被氧化生成氯气;
(3)若X为锌,开关K置于M处,锌为负极,被氧化,铁为正极,发生还原反应.
解答:解:(1)使铜与稀硫酸反应生成硫酸铜与氢气,应设计成电解池,铜为阳极,电解质溶液为硫酸,阴极可为碳,装置图为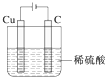 ,
,
故答案为: ;
;
(2)①发生吸氧腐蚀,石墨为正极,氧气得电子被还原生成OH-,方程式为O2+2H2O+4e-═4OH-,
故答案为:O2+2H2O+4e-═4OH-;
②成为钢铁电化学防护的装置,铁连接电源的负极,如图 ,
,
故答案为: ;
;
③形成电解池反应,石墨为阳极,氯离子被氧化生成氯气,方程式为2Cl--2e-═Cl2↑,
故答案为:2Cl--2e-═Cl2↑;
(3)若X为锌,开关K置于M处,锌为负极,被氧化,铁为正极,发生还原反应,为牺牲阳极的阴极保护法(或牺牲阳极保护法),
故答案为:牺牲阳极的阴极保护法(或牺牲阳极保护法).
 ,
,故答案为:
 ;
;(2)①发生吸氧腐蚀,石墨为正极,氧气得电子被还原生成OH-,方程式为O2+2H2O+4e-═4OH-,
故答案为:O2+2H2O+4e-═4OH-;
②成为钢铁电化学防护的装置,铁连接电源的负极,如图
 ,
,故答案为:
 ;
;③形成电解池反应,石墨为阳极,氯离子被氧化生成氯气,方程式为2Cl--2e-═Cl2↑,
故答案为:2Cl--2e-═Cl2↑;
(3)若X为锌,开关K置于M处,锌为负极,被氧化,铁为正极,发生还原反应,为牺牲阳极的阴极保护法(或牺牲阳极保护法),
故答案为:牺牲阳极的阴极保护法(或牺牲阳极保护法).
点评:本题综合考查原电池和电解池知识,综合考查学生的分析能力和综合运用基本理论的能力,注意把握电化学工作原理和电极反应,为解答该题的关键,难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 (2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的.
(2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的. 研究化学反应原理对于生产、生活及环境保护具有重要意义.
研究化学反应原理对于生产、生活及环境保护具有重要意义.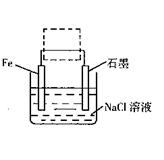
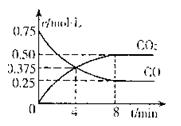

 Fe(s)+CO2(g)。
Fe(s)+CO2(g)。 Fe(s)+CO2(g)
Fe(s)+CO2(g) (CO)= 。
(CO)= 。