题目内容
下列说法正确的是
- A.硅酸钠溶液的保存和碱溶液一样,存放在橡胶塞密封的广口试剂瓶中
- B.

用如图所示操作配制浓硫酸和浓硝酸的混酸 - C.用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管
- D.欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至溶液表面出现晶膜后冷却,过滤得硝酸钾晶体;将滤液加热至有大量晶体析出后,用余热蒸干,得氯化钠晶体
D
分析:A.溶液放在细口瓶中;
B.应将浓硫酸倒入浓硝酸中;
C.移液管取液,垂直放入稍倾斜的容器,管尖与容器内壁不接触,使液体流出;
D.硝酸钾的溶解度受温度影响大,利用冷却热饱和溶液的方法析出硝酸钾.
解答:A.硅酸钠溶液具有粘合性,其保存和碱溶液一样,存放在橡胶塞密封的细口试剂瓶中,故A错误;
B.配制浓硫酸和浓硝酸的混酸,应将浓硫酸倒入浓硝酸中,图中装置会导致液体飞溅,故B错误;
C.用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁不接触,松开食指使溶液全部流出,数秒后,取出移液管,故C错误;
D.硝酸钾的溶解度受温度影响大,则分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至溶液表面出现晶膜后冷却,过滤得硝酸钾晶体;将滤液加热至有大量晶体析出后,用余热蒸干,得氯化钠晶体,故D正确;
故选D.
点评:本题考查化学实验方案的评价,涉及试剂的保存、混合溶液的配制、取液体的方法、混合物的分离,侧重实验基础知识的技能的考查,题目难度中等.
分析:A.溶液放在细口瓶中;
B.应将浓硫酸倒入浓硝酸中;
C.移液管取液,垂直放入稍倾斜的容器,管尖与容器内壁不接触,使液体流出;
D.硝酸钾的溶解度受温度影响大,利用冷却热饱和溶液的方法析出硝酸钾.
解答:A.硅酸钠溶液具有粘合性,其保存和碱溶液一样,存放在橡胶塞密封的细口试剂瓶中,故A错误;
B.配制浓硫酸和浓硝酸的混酸,应将浓硫酸倒入浓硝酸中,图中装置会导致液体飞溅,故B错误;
C.用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁不接触,松开食指使溶液全部流出,数秒后,取出移液管,故C错误;
D.硝酸钾的溶解度受温度影响大,则分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至溶液表面出现晶膜后冷却,过滤得硝酸钾晶体;将滤液加热至有大量晶体析出后,用余热蒸干,得氯化钠晶体,故D正确;
故选D.
点评:本题考查化学实验方案的评价,涉及试剂的保存、混合溶液的配制、取液体的方法、混合物的分离,侧重实验基础知识的技能的考查,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法研究反应速率的有关问题.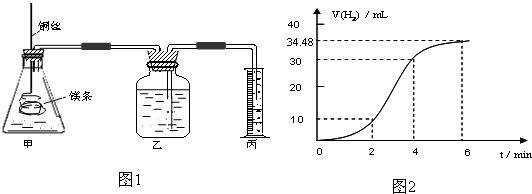
(1)实验1 探究Mg与盐酸反应速率的变化规律.取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是 .(填代号)
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为 .(假设图2氢气体积均已换算为标准状况下的体积,且溶液体积变化可忽略)
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响
已知MnO2+H2O2+2H+═Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
①上表中V1= mL,V3= mL.
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是 .
③若实验测得t2>t3>t4,则可得出的实验结论是 .

(1)实验1 探究Mg与盐酸反应速率的变化规律.取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响
已知MnO2+H2O2+2H+═Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是
③若实验测得t2>t3>t4,则可得出的实验结论是


 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.