题目内容
关于化合物xNa2CO3?yH2O2的推理不正确的是( )A.若1mol该化合物受热完全分解后余下固体212g,则x=y=3
B.若向其滴加稀硫酸有无色气体生成,则该气体可能含有O2和CO2
C.若向其新制溶液中滴加酸性高锰酸钾溶液后褪色,则其溶液具有还原性
D.若向其新制溶液中滴加酚酞后溶液先变红后褪色,则其溶液具有碱性和漂白性
【答案】分析:A、依据完全分解后余下固体212g为碳酸钠计算分析;
B、稀硫酸和碳酸钠反应生成二氧化碳,过氧化氢分解生成氧气;
C、过氧化氢具有还原性;
D、碳酸钠溶液水解显碱性,过氧化氢具有氧化性具有漂白性;
解答:解:A、xNa2CO3?yH2O2加热后变为212 g Na2CO3,所以x=2,y的值无法计算,故A错误;
B、Na2CO3与酸反应产生CO2,H2O2分解会产生O2,所以可能是二氧化碳和氧气,故B正确;
C、因为含有H2O2,O是-1价,为O的中间价态,同时具有氧化性、还原性,可以被高锰酸钾溶液氧化,故C正确;
D、Na2CO3溶液水解呈碱性,H2O2有氧化性,因此H2O2具有漂白性,故D正确;
故选A.
点评:本题考查物质性质的分析应用,氧化还原反应和盐类水解的判断是解题关键,题目难度中等.
B、稀硫酸和碳酸钠反应生成二氧化碳,过氧化氢分解生成氧气;
C、过氧化氢具有还原性;
D、碳酸钠溶液水解显碱性,过氧化氢具有氧化性具有漂白性;
解答:解:A、xNa2CO3?yH2O2加热后变为212 g Na2CO3,所以x=2,y的值无法计算,故A错误;
B、Na2CO3与酸反应产生CO2,H2O2分解会产生O2,所以可能是二氧化碳和氧气,故B正确;
C、因为含有H2O2,O是-1价,为O的中间价态,同时具有氧化性、还原性,可以被高锰酸钾溶液氧化,故C正确;
D、Na2CO3溶液水解呈碱性,H2O2有氧化性,因此H2O2具有漂白性,故D正确;
故选A.
点评:本题考查物质性质的分析应用,氧化还原反应和盐类水解的判断是解题关键,题目难度中等.

练习册系列答案
相关题目
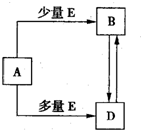 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).