题目内容
从植物的种子或花里提取油宜采用的方法是( )
| A、加氢氧化钠溶液溶解后分液 |
| B、加盐酸一起蒸馏 |
| C、加水溶解后分液 |
| D、加有机溶剂后分液 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作,化学应用
分析:从植物的种子或花果提取油,为油脂的提取,油易溶于有机溶剂而不易溶于水,可利用萃取分离,以此来解答.
解答:
解:从植物的种子或花果提取油,为油脂的提取,因油易溶于有机溶剂而不易溶于水,则加有机溶剂后萃取、分液得到油,常温下油脂不溶于酸、碱,
故选D.
故选D.
点评:本题考查萃取的应用,把握物质的成分、性质及萃取的原理为解答的关键,注意常见物质的溶解性,题目难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列叙述中,不正确的是( )
| A、石英可用来制作工艺品 |
| B、硅单质可用来制造太阳能电池 |
| C、硅单质是制造玻璃的主要原料 |
| D、二氧化硅是制造光导纤维的材料 |
下列有关化学反应速率的说法中,正确的是( )
| A、往容积一定的容器中再通入O2,可以加快反应2SO2+O2?2SO3的反应速率 |
| B、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C、对于C(s)+H2O(g)?CO(g)+H2(g)的反应,加入固体炭,反应速率加快 |
| D、100mL 2mol?L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
下列变化中,由加成反应引起的是( )
| A、将乙醇蒸汽通过灼热的氧化铜,固体颜色由黑色变为红色 |
| B、苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷 |
| C、一定条件下,将苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成 |
| D、往溴水中加入四氯化碳溶液,水层褪色 |
下列反应中,属于加成反应的是( )
A、CH3-CH3+Br2
| |||
B、2CH3CHO+O2
| |||
| C、CH3-CH═CH2+Br2→CH3-CHBr-CH2Br | |||
D、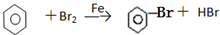 |
在水溶液中,因发生水解反应而不能大量共存的一组离子是( )
| A、CO32-、OH-、Na+、H+ |
| B、Al3+、Na+、AlO2-、Cl- |
| C、Ba2+、HCO3-、K+、SO42- |
| D、S2-、H+、SO42-、Cu2+ |
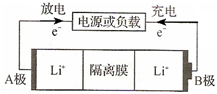 如图为摇摆电池的工作原理图,在充放电过程中Li+在两极间“摇来摇去”,其总反应为:LiCoO2+6C
如图为摇摆电池的工作原理图,在充放电过程中Li+在两极间“摇来摇去”,其总反应为:LiCoO2+6C | 充电 |
| 放电 |
| A、放电时,负极反应为:LiCoO2-═Li(1-x)CoO2+xLi+ |
| B、充电时,B极发生还原反应 |
| C、充电时,Li+穿过隔离膜向B极移动 |
| D、当A极得到x mol电子,电池消耗6 mol C |




