��Ŀ����
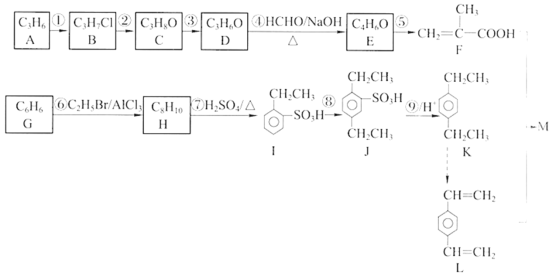
����Ŀ����ϩ���������ʹ㷺���ڽ�������װ���ϵȣ���ϩ���Ǻϳɱ�ϩ������ԭ��֮һ����ϩ���������������͡����ϵȡ��Ա�ϩȩΪԭ��������ϩ������ϩ���������ͼ��ʾ��

��֪��
��2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
��2CH2=CHOONa+H2SO4��2CH2=CHCOOH+Na2SO4
���й����ʵ�������������
���� | ��ϩȩ | ��ϩ�� | ��ϩ�� | ���Ȼ�̼ |
�е�/�� | 53 | 97 | 141 | 77 |
�۵�/�� | - 87 | - 129 | 13 | -22.8 |
�ܶ�/g��mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
�ܽ���(����) | ������ˮ���л��ܼ� | ����ˮ���л��ܼ� | ����ˮ���л��ܼ� | ������ˮ |
(1)��������Ҫ��������30min������װ����ͼ��ʾ������L������________��

(2)������ʹ�õ���Ҫ�����Ƿ�Һ©������ʹ��֮ǰ����еIJ����� ___��
(3)�����ܰ���____�����ˡ���ˮϴ�ӡ��������ɡ�
(4)�������У����������²�Һ�塱����������Ȼ�̼���ٷ������ϩ��(��ͼ)��Ҫ�õ���ϩ��Ӧ�ռ� ____(���¶�)����֡�ͼ����һ�����Դ���Ӧ��Ϊ____��

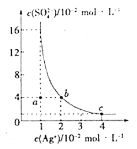
(5)�ⶨ��ϩ����Ħ��������ȷ��ȡamL��ϩ���ڷ�Һ©���У���ƿ��ʢװ����������ʵ��ǰ������B�ж���Ϊb mL������ϩ����ȫ��Ӧ����ȴ�����¡���ƽB��CҺ�棬������B�Ķ���Ϊc mL����֪����������Ħ�����ΪVL��mol-1��

��ƽB��CҺ��IJ�����____��ʵ���ñ�ϩ����Ħ������Ϊ____g��mol-1(�ô���ʽ��ʾ)���������ʱC��Һ�����B�ܣ���ý����____(�ƫ��ƫС�����䡱)��
���𰸡������� ��© ��ˮԡ��ȴ�ᾧ 97�� �¶ȼ�ˮ������������ƿ֧�ܿڴ�����ƽ �����ƶ�C�� ![]() ƫ��
ƫ��
��������
��ϩȩ������������Һ�������ɱ�ϩ���ͱ�ϩ���ƣ��������Ȼ�̼��ȡδ��Ӧ�ı�ϩȩ�ͱ�ϩ�������Ȼ�̼�ܶȱ�ˮ�����Եõ����ϲ�Һ�庬�б�ϩ���ƣ����������ữ�õ���ϩ����Һ����ϩ���۵�Ϊ13�棬���ñ�ˮ��ȴ�ɵõ���ϩ�ᾧ�壬���ˡ���ˮϴ�ӡ��������ɵõ���ϩ��²�Һ��Ϊ��������δ��Ӧ�ı�ϩȩ�����ɵı�ϩ�������Ȼ�̼��Һ������õ���ϩ����
(1)����L�Ľṹ�ص��֪��Ϊ���������ܣ�
(2)���̢�Ϊ��ȡ��Һ����Һ©��ʹ��ǰ��Ҫ���м�©��
(3)���ݷ�����֪�����ܰ�����ˮԡ��ȴ�ᾧ�����ˡ���ˮϴ�ӡ��������ɣ�
(4)������Ŀ��Ϣ��֪��ϩ���ķе�Ϊ97�棬�����ռ�97�����֣���������ʱ�¶ȼƵ�ˮ����Ӧ��������ƿ��֧�ܿڴ���ƽ��
(5)��ϩ�������ǻ��������Ƶ��ʷ�Ӧ����������ͨ���ⶨ���ɵ�����������ȷ����ϩ�������ʵ������Ӷ��ⶨ��Ħ����������¼�������ʱҪע��ͨ�������ƶ�C��ʹB��CҺ��߶�һ�£��Ӷ�ʹ�����ѹǿ�����ѹ��ͬ���õ����������ΪcmL������������Ħ�����ΪVL��mol-1�������ɵ��������ʵ���Ϊ![]() ����ϩ�������к���һ���ǻ������Ա�ϩ�������ʵ���Ϊ
����ϩ�������к���һ���ǻ������Ա�ϩ�������ʵ���Ϊ![]() ����ϩ�����ܶ�Ϊ0.85 g��mL-3����amL��ϩ��������Ϊ0.85ag�����Ա�ϩ����Ħ������Ϊ
����ϩ�����ܶ�Ϊ0.85 g��mL-3����amL��ϩ��������Ϊ0.85ag�����Ա�ϩ����Ħ������Ϊ ��������ʱC��Һ�����B�ܣ���B��ѹǿҪ���ڴ���ѹ�����²�õ��������ƫС�����ݼ��㹫ʽ��֪�ᵼ�¼���õ���Ħ������ƫ��
��������ʱC��Һ�����B�ܣ���B��ѹǿҪ���ڴ���ѹ�����²�õ��������ƫС�����ݼ��㹫ʽ��֪�ᵼ�¼���õ���Ħ������ƫ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�