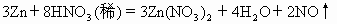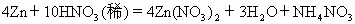题目内容
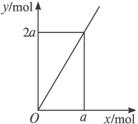
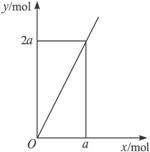
锌与不同浓度的硝酸可发生不同的反应,其中锌与被还原的HNO3的物质的量的关系如下图所示,Y表示消耗Zn的物质的量,X表示被还原的HNO3的物质的量,符合该图的反应是 ( )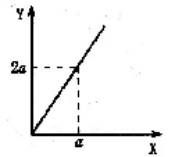
A.3Zn+8HNO3=3Zn(NO3)2+4H2O+2NO↑
B.4Zn+10HNO3=4Zn(NO3)2+5H2O+N2O↑
C.4Zn+10HNO3=4Zn(NO3)2+3H2O+NH4NO3
D.Zn+4HNO3=Zn(NO3)2+2H2O+2NO2↑
答案:B
提示:
提示:
| 由图像可知,每消耗 2mol Zn(失4mole-),则有1mol
HNO3被还原。由得失电子数相等可知,HNO3的还原产物为N2O。
|

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
 3Zn(NO3)2+4H2O+2NO↑
3Zn(NO3)2+4H2O+2NO↑