题目内容
现有可逆反应:2SO2(g) + O2(g) ![]() 2SO3(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措施。
2SO3(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措施。
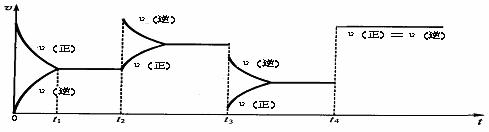 |
t2: ; t3: ; t4: 。
t2 :增大生成物SO3的浓度;
t3 :降低压强;
t4 :加入催化剂

练习册系列答案
相关题目
在一定温度的恒容容器中进行可逆反应:2SO2+O2?2SO3,达到平衡状态的标志是( )
| A、容器中SO2、O2、SO3的分子数之比为2:1:2 | B、容器内气体的密度不随时间而变化 | C、容器内气体的压强不随时间而变化 | D、生成SO3和生成O2的速率相同 |
现有可逆反应:2A(g)+2B(g)?C(g)+3D(g),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
Ⅰ.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下说法中不正确的是( )
| A、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同 | B、Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 | C、达到平衡时,Ⅰ途径A的平衡浓度等于Ⅱ途径A的平衡浓度 | D、达到平衡时,Ⅰ途径所得混合气密度为Ⅱ途径所得混合气密度的2倍 |