题目内容
在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间t的变化如下表
2NO2(g)体系中,n(NO)随时间t的变化如下表
 2NO2(g)体系中,n(NO)随时间t的变化如下表
2NO2(g)体系中,n(NO)随时间t的变化如下表
(1)写出该反应的平衡常数表达式:K=__________。已知平衡常数K300℃>K350℃,则该反应是________热反应。
(2)下图中可用来表示NO2的变化的曲线是________(填字母)。用O2表示从0~2s内该反应的平均速率v=________。
(2)下图中可用来表示NO2的变化的曲线是________(填字母)。用O2表示从0~2s内该反应的平均速率v=________。

(3)能说明该反应已达到平衡状态的是____。
a.v(NO2)=2v(O2) b.容器内压强保持不变 c.v逆(NO)=2v正(O2) d. 容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
a.及时分离出NO2气体 b.适当升高温度 c. 增大O2的浓度 d. 选择高效催化剂
a.v(NO2)=2v(O2) b.容器内压强保持不变 c.v逆(NO)=2v正(O2) d. 容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
a.及时分离出NO2气体 b.适当升高温度 c. 增大O2的浓度 d. 选择高效催化剂
(1)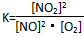 ;放
;放
(2)b;1.5×10-3 mol·L-1·s-1
(3)bc
(4)c
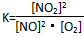 ;放
;放(2)b;1.5×10-3 mol·L-1·s-1
(3)bc
(4)c

练习册系列答案
相关题目
一定条件下,使X(g)与Y(g)在2L密闭容器中发生反应生成z(g).温度为TK时,反应过程中X,Y,Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T,K和T2,K时,Y的体积分数与时间的关系如图2所示.则下列结论正确的是( )
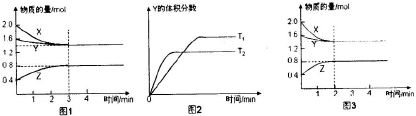

| A、反应进行的前3min内,用X表示的反应速率V(X)=0.1mol/(L?min) | B、平衡时容器内的压强为反应前的0.8倍 | C、保持其他条件不变,升高温度,反应的化学平衡常数K减小 | D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
某温度(t℃)时,在2L密闭容器内发生反应:2A (g)+B(g)?2C(g)体系中n(A)随时间的变化如下表:
请回答:
(1)用A浓度变化表示从0~2s内该反应的平均速率v= mol/.
(2)能说明该反应已达到化学平衡状态的是 (填序号).
①容器内压强保持不变 ②A的物质的量保持不变
③容器内密度保持不变 ④消耗2mol A的同时,消耗1mol B
(3)温度升高,A的转化率减小,则该正反应是 (填“吸热”或“放热”)反应.
(4)若开始时充入B的物质的量是A的一半,则t℃时平衡常数K的数值是 .
| 时间/s | 1 | 2 | 3 | 4 | |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
(1)用A浓度变化表示从0~2s内该反应的平均速率v= mol/.
(2)能说明该反应已达到化学平衡状态的是 (填序号).
①容器内压强保持不变 ②A的物质的量保持不变
③容器内密度保持不变 ④消耗2mol A的同时,消耗1mol B
(3)温度升高,A的转化率减小,则该正反应是 (填“吸热”或“放热”)反应.
(4)若开始时充入B的物质的量是A的一半,则t℃时平衡常数K的数值是 .