题目内容
在饱和碳酸钠溶液中加入稀盐酸,边加入边搅拌,最初无气体产生,溶液变浑浊,其原因是________,化学反应方程式为________.继续滴入稀盐酸有气体放出,溶液变澄清,其原因是________,化学反应方程式为________.
答案:
解析:
解析:
答案:Na2CO3与盐酸反应生成NaHCO3,相同条件下NaHCO3溶解度比Na2CO3小;Na2CO3+HCl=NaHCO3+NaCl;NaHCO3与盐酸反应生成CO2气体和NaCl、NaCl溶解度比Na2CO3大;NaHCO3+HCl=NaCl+CO2↑+H2O.
解析:Na2CO3的溶解度大于相同条件下NaHCO3的溶解度,当在饱和Na2CO3溶液中滴加稀盐酸时,发生反应:Na2CO3+HCl=NaCl+NaHCO3而析出NaHCO3晶体.继续加入盐酸时发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,NaCl溶解度较大,溶液澄清,生成CO2气体.
评注:一般正盐的溶解度比酸式盐小,但NaHCO3例外.

练习册系列答案
相关题目
 CH3COOCH2CH3+H2O
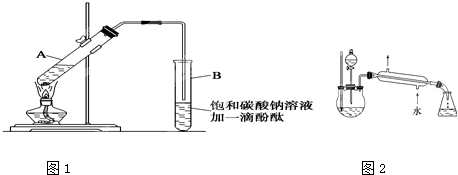
CH3COOCH2CH3+H2O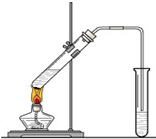 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: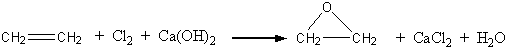


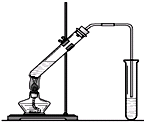 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: