题目内容
有两种金属的合金12g,与足量稀硫酸反应后,在标准状况下产生气体11.2L,则组成该合金的金属可能是( )
| A、Mg和Al | B、Cu和Zn | C、Fe和Zn | D、Al和Fe |
分析:假设金属与硫酸反应都为+2价,根据M=
计算金属混合物的平衡相对原子质量,利用平均值法判断.
| m |
| n |
解答:解:标准状况下11.2L氢气的物质的量为
=0.5mol,
假设金属都为+2价,根据电子转移守恒可知,金属的物质的量为0.5mol,则金属混合物的平均相对原子质量为24,
A.Mg的相对原子质量为24,当Al的化合价为+2价时,可看成其相对原子质量为
×27=18,二者平均相对原子质量介于18~24之间,小于金属混合物的平均相对原子质量为24,故A错误;
B.Cu不反应,其的相对原子质量看做无穷大,Zn的相对原子质量为65,二者平均相对原子质量大于24,故B错误;
C.Fe的相对原子质量为56,Zn的相对原子质量为65,二者平均相对原子质量介于56~65之间,大于金属混合物的平均相对原子质量为24,故C错误;
D.当Al的化合价为+2价时,可看成其相对原子质量为
×27=18,Fe的相对原子质量为56,二者平均相对原子质量介于18~56之间,可能为24,符合题意,故D正确,
故选D.
| 11.2L |
| 22.4L/mol |
假设金属都为+2价,根据电子转移守恒可知,金属的物质的量为0.5mol,则金属混合物的平均相对原子质量为24,
A.Mg的相对原子质量为24,当Al的化合价为+2价时,可看成其相对原子质量为
| 2 |
| 3 |
B.Cu不反应,其的相对原子质量看做无穷大,Zn的相对原子质量为65,二者平均相对原子质量大于24,故B错误;
C.Fe的相对原子质量为56,Zn的相对原子质量为65,二者平均相对原子质量介于56~65之间,大于金属混合物的平均相对原子质量为24,故C错误;
D.当Al的化合价为+2价时,可看成其相对原子质量为
| 2 |
| 3 |
故选D.
点评:本题考查混合物的计算,题目难度中等,侧重解题方法技巧与思维能力考查,利用平均值法可快速解答,注意化合价与相对原子质量的转化.

练习册系列答案
相关题目
Ⅰ.配平下列反应方程式:
NaIO3+ NaHSO3-- I2+ Na2SO4+ H2SO4+ H2O
Ⅱ.废旧金属的回收再利用是保护自然资源的有力措施.一批成分不详的合金废料,为了确定其成分和再利用途径,探究性学习小组拟定以下方案进行实验分析:
请回答下列问题:
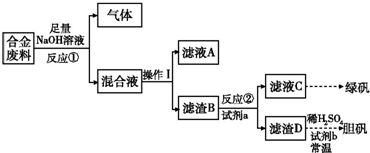
(1)从上述信息知,该合金中可确定的成分有 ;(填化学式)
(2)滤渣D中加入稀硫酸和试剂b,常温下可制得胆矾,是一种绿色化学工艺,则试剂b是 ;写出总反应方程式 ;
(3)甲、乙两同学都验证了反应①生成气体是氢气,甲同学推断滤液A应是NaAlO2;乙同学查阅资料得知硅与NaOH溶液反应也有H2放出,因此持不同意见,请你设计一最佳方案,帮助他们作一确证:(写出选用试剂、实验判断现象及得出结论)
(4)取质量均为m g的滤渣B四份,分别加入同浓度,不同体积的稀HNO3充分反应,在标准状况生成NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
①实验1溶解的金属是 ;质量为 g;
②写出实验4中金属恰好溶解后,发生反应的离子方程式: .实验4中V的数值为 .
Ⅱ.废旧金属的回收再利用是保护自然资源的有力措施.一批成分不详的合金废料,为了确定其成分和再利用途径,探究性学习小组拟定以下方案进行实验分析:
请回答下列问题:

(1)从上述信息知,该合金中可确定的成分有
(2)滤渣D中加入稀硫酸和试剂b,常温下可制得胆矾,是一种绿色化学工艺,则试剂b是
(3)甲、乙两同学都验证了反应①生成气体是氢气,甲同学推断滤液A应是NaAlO2;乙同学查阅资料得知硅与NaOH溶液反应也有H2放出,因此持不同意见,请你设计一最佳方案,帮助他们作一确证:(写出选用试剂、实验判断现象及得出结论)
(4)取质量均为m g的滤渣B四份,分别加入同浓度,不同体积的稀HNO3充分反应,在标准状况生成NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | 1 | 2 | 3 | 4 |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L) | 1.12 | 2.24 | 3.36 | V |
②写出实验4中金属恰好溶解后,发生反应的离子方程式: