��Ŀ����
3�������仯�����й㷺Ӧ�ã��ش��������⣮��1��������һ����Ҫ�Ĺ�ҵԭ�ϣ���ҵ�����õ�����������һ�������ºϳɰ�����N2��g��+3H2��g��?2NH3��g����H���÷�Ӧ�����е������仯��ͼ1��ʾ��E1��0��E2��0����
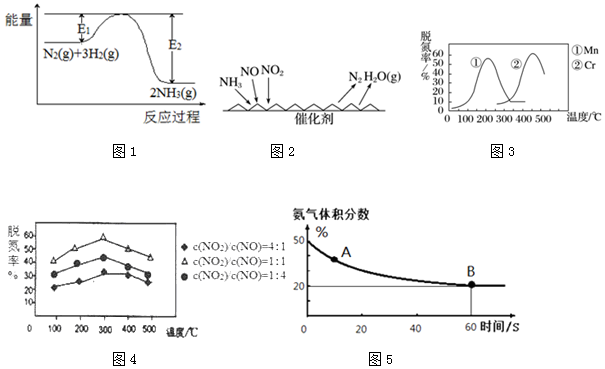
ͼ��E1�����������Ƿ�Ӧ��Ļ�ܣ���Ӧ�ȡ�H�ı���ʽΪE1-E2 ����E1��E2��ʾ����
��2��NH3����ԭ�������SCR��������ĿǰӦ����㷺���������������ѳ���������Ӧԭ����ͼ2��ʾ��
��ͼ3�Dz�ͬ����Mn��Cr�ڲ�ͬ�¶��¶�Ӧ���ѵ��ʣ���ͼ�ۺϿ��ǿ�֪��ѵĴ�������Ӧ���¶ȷֱ�ΪMn��200-250�森
����Fe������ʱ���ڰ�������������£���ͬc��NO2��/c��NO����Ӧ���ѵ�����ͼ4��ʾ���ѵ�Ч����ѵ�c��NO2��/c��NO��=1��1����֪����11.2L N2������£���Ӧ�ų�������ΪQ kJ����ʱ��Ӧ���ѵ���Ӧ���Ȼ�ѧ����ʽΪ2NH3��g��+NO��g��+NO2��g��?2N2��g��+3H2O��g����H=-4QkJ/mol��
��3����ҵ�Ϻϳ����صķ�Ӧ��2NH3��g��+CO2��g��?H2O��g��+CO��NH2��2 ��l����H��
��һ����պ����ܱ������г���CO2��NH3����������Ӧ���㶨�¶��»��������NH3�����������ͼ5��ʾ��
A�������Ӧ����v����CO2����B����淴Ӧ����v����CO2�������������������=������CO2��ƽ��ת����Ϊ37.5%��
��4����ҺҲ�ܷ��磡��ѧ�������о����ض���ȼ�ϵ�أ������ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ���ܷ��磬���ع���ԭ��Ϊ2CO��NH2��2+3O2�T2N2+2CO2+4H2O���������ҺΪ���ᣬ���ĵ缫��ӦʽΪCO��NH2��2+H2O-6e-=CO2+N2+6H+��
���� ��1��E1�����������Ƿ�Ӧ��Ļ�ܣ���Ӧ�з�Ӧ��������������������������Ӧ�Ƿ��ȷ�Ӧ���ʱ�С���㣬�����ʱ�ĺ������ش�
��2�����¶�Խ�ߣ����豸��Ҫ��Խ�ߣ�������������ڽϵ��¶����ܽϴ�̶ȵ����⼴�ɣ������������жϣ���ͬ�¶��£�������Խ�ߵ�Ч��Խ�ã�
�ھ�ͼ����з������ѵ�Ч����ѵ�c��NO2��/c��NO��=1��1������1mol�����ų�QkJ������������2mol�����ų�2QkJ������
��3��ͼ��������������������50%�仯Ϊ20%������������ֲ��䣬˵��B�㷴Ӧ�ﵽƽ��״̬��A�㰱������ٷֺ�������B�İ�������ٷֺ�����˵����Ӧ������дﵽƽ��״̬��A�������Ӧ���ʴ���B�������Ӧ���ʣ����ݰ���������������ƽ������ʽ��ʽ����ƽ��ת���ʣ�
��4��������ȼ�ϵ�صĽṹ��֪�������������õ���������ˮ������������ʧȥ�������ɵ����Ͷ�����̼��
��� �⣺��1��E1�����������Ƿ�Ӧ��Ļ�ܣ�����ͼ����Ϣ�õ�����Ӧ��������������������������Ӧ�Ƿ��ȷ�Ӧ���ʱ�=���������-��Ӧ���������ͼ�У�E1����ͨ���ӱ�Ϊ��������յ�������E2 �ǻ����֮��ķ�Ӧ���ɲ���������仯��E1-E2 �Ƿ�Ӧ��Ͳ��������֮���Ӧ�Ƿ��ȵģ������ʱ�=E1-E2 ��0��
�ʴ�Ϊ����Ӧ��Ļ�ܣ�E1-E2 ��
��2���ٸ���ͼ��֪��������Խ��Խ�ã���Cr������ʱ�¶ȸ���Mn���¶�Խ�ߣ����豸Ҫ��Խ�ߣ����������ɱ����������������С������ʹ��Mn�������Ϻã�����ͼ��֪�����¶�Ϊ200-250���Χ�ڼ������¶ȣ������ʽϸߣ�
�ʴ�Ϊ��Mn��200-250�棻
�ھ�ͼ����з������ѵ�Ч����ѵ�c��NO2��/c��NO��=1��1������0.5mol�����ų�QkJ������������2mol�����ų�4QkJ�����������Ȼ�ѧ��Ӧ����ʽΪ2NH3��g��+NO��g��+NO2��g��?2N2��g��+3H2O��g����H=-4QkJ/mol��
�ʴ�Ϊ��1��1��2NH3��g��+NO��g��+NO2��g��?2N2��g��+3H2O��g����H=-4QkJ/mol��
��3�����������������50%�仯Ϊ20%������������ֲ��䣬˵��B�㷴Ӧ�ﵽƽ��״̬��A�㰱������ٷֺ�������B�İ�������ٷֺ�����˵����Ӧ������дﵽƽ��״̬��A�������Ӧ���ʴ���B�������Ӧ���ʣ���v����CO2����v����CO2����
�谱��Ϊ50mol��������̼Ϊ50mol���������ĵ����ʵ���x����ʼ�����������Ϊ50%����
2NH3��g��+CO2��g��?CO��NH2��2��s��+H2O��g��
��ʼ����mol�� 50 50 0 0
�仯����mol�� x 0.5x 0.5x 0.5x
ƽ������mol�� 50-x 50-0.5x 0.5x 0.5x
ƽ��ʱ�������������Ϊ20%����$\frac{50-x}{50-0.5x+50-x+0.5x}$=20%�����x=37.5mol��
��CO2��ƽ��ת����=$\frac{0.5��37.5mol}{50mol}$=37.5%��
�ʴ�Ϊ������37.5%��
��4��������ȼ�ϵ�صĽṹ��֪������������ʧȥ�������ɵ����Ͷ�����̼��������ӦΪCO��NH2��2+H2O-6e-=CO2+N2+6H+��
�ʴ�Ϊ��CO��NH2��2+H2O-6e-=CO2+N2+6H+��
���� ���⿼�黯ѧƽ����㼰ԭ��ء���Ӧ�ȵȣ�Ϊ��Ƶ���㣬���ջ�ѧƽ�����η���ת���ʵļ��㡢�缫��ӦΪ���Ĺؼ������ط�������������Ŀ��飬ע��ƽ���ƶ�ԭ����Ӧ�ã���Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | �����£�10 mL 0.2mol/L NH4NO3��Һ��10 mL 0.1mol/L NaOH��Һ��Ϻ�����pH=9.6����Һ�У�c��NO3-����c��NH4+����c��Na+����c��NH3•H2O����c��OH-����c��H+�� | |
| B�� | 0.1 mol/LNa2S��Һ�У�c��Na+��+c��H+��=c��S2-��+c��HS-��+c��OH-�� | |
| C�� | ������a mL 0.1 mol/L KOH��b mL 0.1 mol/L HCN����Һ��Ϻ�pH��7������a��b��a��b | |
| D�� | 10 mL 0.1mol/L NaCl��Һ����������Ϊx��10mL 0.1mol/L CH3COONa��Һ����������Ϊy����x��y |
��NaHCO3
��Al2O3
��Al��OH��3
��Al
�ݣ�NH4��2CO3��
| A�� | �٢ۢܢ� | B�� | �ڢۢܢ� | C�� | �٢ڢۢ� | D�� | ȫ�� |
| A�� | A��B��Eһ������ͬһ���� | B�� | DΪ�ڶ�����Ԫ�� | ||
| C�� | A��D��������ͬһ���� | D�� | B��D������ͬһ���� |
| A�� | ԭ�Ӱ뾶��С��X��Y��Z��T��W | |
| B�� | ��Ԫ������a��MgS��������H2S | |
| C�� | Ԫ��Z�ĵ���������Ԫ�صĵ��ʶ����Է�����ѧ��Ӧ | |
| D�� | �ǽ����ԣ�Z��W��T |
| A�� | �춡�������ԭ�Ӷ�λ��ͬһƽ���� | |
| B�� | ������ˮ��Ӧ��ȡ�屽���ڼӳɷ�Ӧ | |
| C�� | ����������������ˮ������Ϊ������ | |
| D�� | �һ��������һ�������6�� |
| A�� | ����NH4Clֻ�ƻ����Ӽ� | |
| B�� | N2H4�м��Լ���Ǽ��Լ��ı�ֵ��1��4 | |
| C�� | PCl3��BCl3����������ԭ�ӵ�����㶼�ﵽ8�����ȶ��ṹ | |
| D�� | ijԪ������������ˮ������⻯��Ļ�ѧʽ�ֱ�ΪH2XO4��H2X |
| A�� | �٢� | B�� | �ۢ� | C�� | �� | D�� | �٢� |
��������

| A�� | ԭ��Һ��һ��������Ag+��Al3+��Ba2+��SO42- | |
| B�� | ʵ�������ɳ��������ӷ���ʽ��SiO32-+2H+=H2SiO3�� | |
| C�� | ԭ��Һһ������K+��CO32-�����ܴ���NO3- | |
| D�� | ԭ��Һ������NO3-ʱ��c��K+��=0.8mol•L-1 |