题目内容
【题目】已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=![]()
B.对于反应③,恒容时,温度升高,H2浓度减小,则K变大
C.反应③的平衡常数K=![]()
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
【答案】C
【解析】
A. 化学平衡常数表达式中固体、纯液体不需要表示,反应①的平衡常数K1=![]() ,故A错误;
,故A错误;
B. 对于反应③,恒容时,温度升高,H2浓度减小,说明升高温度平衡向逆反应移动,则K=![]() 变小,故B错误;
变小,故B错误;
C. 反应①的平衡常数K1=![]() ,反应②的平衡常数K2=
,反应②的平衡常数K2=![]() ,反应③的平衡常数为K=
,反应③的平衡常数为K=![]() = K1×
= K1×![]() =
=![]() ,故C正确;
,故C正确;
D. 对于反应③,恒温恒容下,通入稀有气体增大压强,容器体积不变,反应体系中各组分的浓度不变,平衡不移动,则H2的浓度不变,故D错误;
答案选C。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】下表是3种物质的溶解度![]() ,下列说法中正确的是
,下列说法中正确的是![]()
物质 |
|
|
|
溶解度 | 74 |
|
|
A.已知![]() 的
的![]()
![]() ,则所有含有固体
,则所有含有固体![]() 的溶液中,都有
的溶液中,都有![]() ,且
,且![]()
![]()
B.除去粗盐中含有的![]() 杂质,最佳除杂试剂为
杂质,最佳除杂试剂为![]() 溶液
溶液
C.将表中三种物质与水混合,加热、灼烧,最终的固体产物相同
D.用石灰水处理含有![]() 和
和![]() 的硬水,发生的离子反应方程式为
的硬水,发生的离子反应方程式为![]()
【题目】某化学兴趣小组借助![]() 的仪器装置完成有关实验。
的仪器装置完成有关实验。

(1)用装置A收集NO气体,正确的操作是 ______ ![]() 填序号
填序号![]() 。
。
a.从①口进气,用排水法集气
b.从①口进气,用排气法集气
c.从②口进气,用排水法集气
d.从②口进气,用排气法集气
(2)B装置中的恒压分液漏斗有两个作用,其一是平衡气压使分液漏斗内的液体能顺利滴下,其另一个作用是 ______。
(3)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是![]() 、
、![]() 或二者混合物。探究过程如下:
或二者混合物。探究过程如下:
查阅资料:
![]() 是一种碱性氧化物,溶于稀硫酸生成Cu和
是一种碱性氧化物,溶于稀硫酸生成Cu和![]() ,在空气中加热生成CuO
,在空气中加热生成CuO
提出假设:
假设1:红色粉末是![]()
假设2:红色粉末是![]()
假设3:红色粉末是![]() 和
和![]() 的混合物
的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
①若滴加KSCN试剂后溶液不变红色,甲同学认为原固体粉末中一定不含三氧化二铁.乙同学认为其结论不正确,乙同学的理由是 ______。
②若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 ______。
![]() 经分析,确定红色粉末为
经分析,确定红色粉末为![]() 和
和![]() 的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾
的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾![]() 。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使
。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使![]() 、
、![]() 、
、![]() 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
物质 |
|
|
|
开始沉淀pH | 6.0 |
|
|
沉淀完全pH | 13 | 14 |
|
实验室有下列试剂可供选择:![]() 氯水
氯水 ![]()
![]()
![]()
实验小组设计如下实验方案:
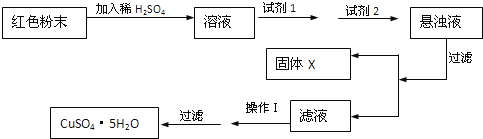
试回答:
①试剂为1____ ![]() 填字母
填字母![]() ,写出溶液中发生反应的离子方程式
,写出溶液中发生反应的离子方程式![]() 写出一个即可
写出一个即可![]() ___。
___。
②试剂为2______ ![]() 填字母
填字母![]() 。
。
③固体X的化学式为 ______。
④操作I为 ______。
【题目】已知某气态化石燃料X中只含有碳、氢两种元素,为探究该气体中碳和氢两种元素的质量比,某同学设计了燃烧法测量的实验方案,通过测量装置C和D的增重即可求得碳和氢两种元素的质量比.实验装置如下图所示![]() 已知CuO可以作为碳氢化合物燃烧的催化剂
已知CuO可以作为碳氢化合物燃烧的催化剂![]() :
:

(1)若A装置中所盛放的药品是浓NaOH溶液,装置A的作用有:
①______;
②______
(2)D装置中所盛放的药品是______,
(3)E装置的作用是______,
(4)上述装置中有一处缺陷,请改正______.
(5)若实验装置经过改正后,得到的实验数据如下:
质量 | 实验前 | 实验后 |
药品 |
|
|
药品 |
|
|
则该气体中碳和氢两种元素的质量比为______.
