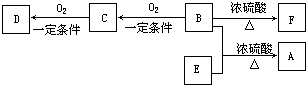
��Ŀ����
14�� A��B��C��D��E��F��ԭ���������������ǰ�����ڵij���Ԫ�أ��������Ϣ���±���
A��B��C��D��E��F��ԭ���������������ǰ�����ڵij���Ԫ�أ��������Ϣ���±���| A | �����к�����ḻ��Ԫ�� |
| B | �����������Ǵ�����������2�� |
| C | ����������Ӧ��ˮ���������⻯�ﷴӦ������ |
| D | ԭ�Ӻ��������8�ֲ�ͬ���˶�״̬ |
| E | ��̬ԭ�Ӻ���������δ�ɶԵ��� |
| F | ԭ�������ֻ��һ������ |
��1����̬Eԭ�ӵĺ���M���������9�ֲ�ͬ����չ����̬Eԭ�Ӻ���۵����Ų�ʽΪ3d54s1��Ԫ��F����d����
��2��A��C�γɵ�����ӵĿռ乹��Ϊ�����Σ�����ԭ�ӵ��ӻ���ʽΪsp3��
��3��B��C��D��һ�������ɴ�С��˳����N��O��C����Ԫ�ط��ű�ʾ������B��C��D�е�����Ԫ����ɵij������ӻ�Ϊ�ȵ��������N2O��CO2
��4��EԪ�ؿ����γ���λ ��Ϊ6�������������ǵĻ�ѧʽ����ECl3�q6H2O������һ�ֳ�����ɫ������������Һ��Ӧʱ���ܳ�����$\frac{1}{3}$����Ԫ�أ��������ɱ�ʾΪ[Cr��H2O��4Cl2]Cl•2H2O��
��5��Ԫ��F��һ���Ȼ���ľ����ṹ��ͼ ��ʾ�������ʾFԭ�ӣ������ʾ��ԭ�ӣ���ÿ����ԭ����Χ��֮�����������ԭ�Ӹ���Ϊ12�����������ܶ�Ϊ4.14g�qcm-3���þ����ı߳�Ϊ$\root{3}{\frac{398}{4.14{N}_{A}}}$cm��ֻҪ������ʽ�����ؼ������ֵ�������ӵ���������ֵΪNA��
���� AΪ�����к�����ḻ��Ԫ�أ���AΪHԪ�أ�B�������������Ǵ�����������2�����������ຬ��8�����ӣ���B����2�����Ӳ㣬�����Ϊ2�����ӣ���BΪCԪ�أ�C������������Ӧ��ˮ���������⻯�ﷴӦ�����Σ���CΪNԪ�أ�D��ԭ�Ӻ��������8�ֲ�ͬ���˶�״̬����ԭ�Ӻ����������Ϊ8��ΪOԪ�أ�E�Ļ�̬ԭ�Ӻ���������δ�ɶԵ��ӣ���E�ĺ�������Ų�ʽΪ��1s22s22p63s23p63d54s1����EΪCrԪ�أ�Fԭ�������ֻ��һ�����ӣ���ԭ����������Cr��ǰ������Ԫ�أ���FΪCuԪ�أ��ݴ˽��н��
��� �⣺AΪ�����к�����ḻ��Ԫ�أ���AΪHԪ�أ�B�������������Ǵ�����������2�����������ຬ��8�����ӣ���B����2�����Ӳ㣬�����Ϊ2�����ӣ���BΪCԪ�أ�C������������Ӧ��ˮ���������⻯�ﷴӦ�����Σ���CΪNԪ�أ�D��ԭ�Ӻ��������8�ֲ�ͬ���˶�״̬����ԭ�Ӻ����������Ϊ8��ΪOԪ�أ�E�Ļ�̬ԭ�Ӻ���������δ�ɶԵ��ӣ���E�ĺ�������Ų�ʽΪ��1s22s22p63s23p63d54s1����EΪCrԪ�أ�Fԭ�������ֻ��һ�����ӣ���ԭ����������Cr��ǰ������Ԫ�أ���FΪCuԪ�أ�
��1��EΪCrԪ�أ���̬Crԭ�ӵĺ���M����ӷ�Ϊ3s��3p����3d������ֱ���1��3��5���������9�ֲ�ͬ����չ����EΪCrԪ�أ���̬ԭ�ӵļ۵����Ų�ʽΪ3d54s1��CrԪ��λ�����ڱ���d����
�ʴ�Ϊ��9��3d54s1��d��
��2��A��C�γɵ������Ϊ�����������Ŀռ乹��Ϊ�����Σ�����ԭ��Nԭ�Ӵ���3�����ۼ���������1���µ��Ӷԣ������ӻ���ʽΪsp3��
�ʴ�Ϊ�������Σ�sp3��
��3��B��C��D�ֱ�ΪC��N��O��ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ�����������������IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ�C��N��OԪ�ش���ͬһ������ԭ������������N���ڵ�VA�壬���Ե�һ������N��O��C��
B��C��D�е�����Ԫ����ɵij������ӻ�Ϊ�ȵ��������N2O��CO2��
�ʴ�Ϊ��N��O��C��N2O��CO2��
��4��EΪ��Ԫ�أ���������ϼ�Ϊ+6�ۣ����������֪���Ȼ�����CrCl3•6H2O�����Ȼ��������ʵ���֮����1��3�������������غ�֪����CrCl3•6H2O��ѧʽ�к���1��������Ϊ������ӣ�ʣ���2������������ԭ�ӣ������Ȼ�����CrCl3•6H2O���Ļ�ѧʽΪ[Cr��H2O��4Cl2]Cl•2H2O��
�ʴ�Ϊ��[Cr��H2O��4Cl2]Cl•2H2O��
��5��FΪCuԪ�أ�Ԫ��F��һ���Ȼ���ľ����ṹ��ͼ��ʾ�������ʾFԭ�ӣ������ʾ��ԭ�ӣ����Ծ������㴦Clԭ��Ϊ�о�������8���������ø�Clԭ�ӣ�ÿ����ԭ���������Clԭ�Ӿ��������ÿ��Clԭ��Ϊ�����������ã�����ÿ����ԭ����Χ��֮�����������ԭ�Ӹ���Ϊ��3��8��$\frac{1}{2}$=12��
�ɾ����ṹ��֪��Cuԭ��λ�������붥���ϣ�������Cuԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��������Clԭ�Ӵ������ڣ�Clԭ�ӵ���ĿΪ4���ʸû�����Ļ�ѧʽΪCuCl��ÿ������������Ϊ��$\frac{99.5}{{N}_{A}}$��4g=$\frac{398}{{N}_{A}}$g���辧���߳�Ϊl�������Ϊ��V=l3=$\frac{\frac{398}{{N}_{A}}}{4.14}$=$\frac{398}{4.14{N}_{A}}$�����Ծ����߳�Ϊ��l=$\root{3}{\frac{398}{4.14{N}_{A}}}$��
�ʴ�Ϊ��12��$\root{3}{\frac{398}{4.14{N}_{A}}}$��
���� ���⿼����λ�á��ṹ�����ʹ�ϵ���ۺ�Ӧ�ã���Ŀ�ۺ��Խϴ��漰�ṹ����Խλ�ù�ϵ��Ԫ�������ɡ���������Ų�����������ӻ����ۡ����ӽṹ�ȣ���Ŀ�Ѷ��еȣ������ʽṹ���ۺ�����Ŀ���Ƕ�ѧ���ۺ������Ŀ��飮

| A�� | �ױ���ʹ���Ը��������Һ��ɫ��������ʹ���Ը��������Һ��ɫ | |
| B�� | �����ܸ�NaOH��Һ��Ӧ���Ҵ�������NaOH��Һ��Ӧ | |
| C�� | ��ϩ�ܷ����ӳɷ�Ӧ�����鲻�ܷ����ӳɷ�Ӧ | |
| D�� | ���������ڼ���ʱ����ȡ����Ӧ���ױ��������ڳ����¾��ܷ���ȡ����Ӧ |
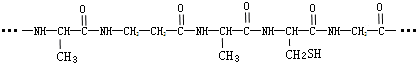
| A�� | 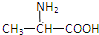 | B�� | H2NCH2COOH | C�� | 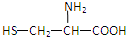 | D�� | 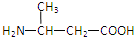 |
| A�� | �ŵ�ʱ��Na+���ƶ� | |
| B�� | �ŵ�ʱ�������Ϸ����ķ�ӦΪxS+2Na++2e-=Na2Sx | |
| C�� | ���ʱ�������Ϸ����ķ�ӦΪ2Na-2e-=2Na+ | |
| D�� | �ŵ�ʱ��ÿ��0.4mol����ת�ƣ�����9.2gNa��6.4g��μӷ�Ӧ |
| A�� | Ԫ��Y��Q���γ�һ�ֻ�����Y2Q3 | |
| B�� | T��һ�ֵ��ʵĿռ���Ϊ���������� | |
| C�� | X��Q������ɵĻ�����Ϊ���ӻ����� | |
| D�� | ZO2�Ǽ��Լ����ɵķǼ��Է��� |
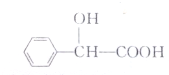 ij�л���Ľṹ������ʾ���йظ����ʵ�˵��������ǣ�������
ij�л���Ľṹ������ʾ���йظ����ʵ�˵��������ǣ�������| A�� | �����ʵķ���ʽΪC8H8O3 | |
| B�� | �����ʷ����е�8��̼ԭ�Ӷ���ͬһ��ƽ���� | |
| C�� | �����ʼȿ��Է���������Ӧ�ֿ��Է������۷�Ӧ | |
| D�� | 1mol�����ʿ�����2mol����Na��Ӧ |
a��0��t1ʱ��v����v����t2ʱ��v����v��
b�����������ܶȲ��ٸı�ʱ���������̴ﵽƽ��
c��t2ʱ�̸ı���������������ܱ������м�C
d���������̴ﵽƽ��ʱ��ƽ�ⳣ����

��2����ҵ�ϳ���CO2��NH3ͨ�����·�Ӧ�ϳ�����[CO��NH2��2]��
CO2��g��+2NH3��g��$\stackrel{һ������}{?}$CO��NH2��2��l��+H2O��g����H��0t��ʱ�����ݻ��㶨Ϊ2L���ܱ������м���0.10molCO2��0.40molNH3��70min��ʼ�ﵽƽ�⣮��Ӧ��CO2�� g�������ʵ�����ʱ��仯�����ʾ��
| ʱ��/min | ��0 | 20 | 70 | 80 | 100 |
| n��CO2��/mol | 0.10 | 0.060 | 0.020 | 0.020 | 0.020 |
����100minʱ�����������������䣬���������г���0.050mo1CO2��0.20molNH3�����½���ƽ���CO2��ת������ԭƽ����Ƚ���������������䡱��С������
���������淴Ӧ��ƽ�ⳣ��Ϊ277.8������һλС������
��ͼ2��ʾװ�ã�����������Ϊ���Ե缫�������ڵ�����ء�CO��NH2��2���ļ�����Һ��ȡ��������װ���������ĵ缫��ӦʽΪCO��NH2��2+8OH--6e-=CO32-+N2��+6H2O��
��3��CH4ȼ�ϵ�أ�װ��ʾ����ͼ3��A��BΪ�����̼����������ͨ����飬�ڱ�״���£����ļ������VL���� 0��V��44.8Lʱ������ܷ�Ӧ����ʽΪCH4+2O2+KOH=KHCO3+2H2O��