题目内容
在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应,放出大量气体,反应过程表示如下:
①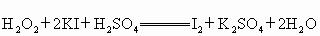 ;
;
②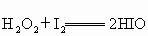 ;
;
③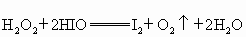
(1)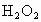 在反应③中__________(填正确选项的标号).
在反应③中__________(填正确选项的标号).
A.是氧化剂
B.是还原剂
C.既是氧化剂又是还原剂
D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为_____________(填“对”或“不对”),其理由是__________________.
(3)上述反应说明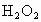 、
、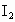 、HIO氧化性从强到弱的顺序是_________.
、HIO氧化性从强到弱的顺序是_________.
(4)已知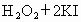
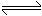
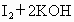 ,试用
,试用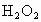 、KI溶液、淀粉溶液、水等药品,设计一个实验来说明与一定量
、KI溶液、淀粉溶液、水等药品,设计一个实验来说明与一定量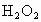 反应的KI溶液浓度越大,反应速率越快.
反应的KI溶液浓度越大,反应速率越快.
_____________________________________________
答案:略
解析:
解析:
|
(1)B (2) 对.从反应②、③可看出碘在反应中没有消耗,在碘的存在下过氧化氢分解放出氧气的速率加快(3)HIO >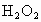 > >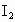
(4) 操作步骤如下:①取两只试管,标明(Ⅰ)、(Ⅱ),分别注入等量的少许淀粉溶液和KI溶液,混合均匀;②在试管(Ⅰ)中加水,使体积变为原来的若干倍;③在两试管中同时滴加等量的同种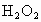 溶液.可发现(Ⅱ)试管内先变蓝. 溶液.可发现(Ⅱ)试管内先变蓝. |

练习册系列答案
相关题目