题目内容
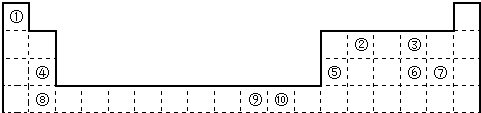
如图为长式周期表的一部分,其中的编号代表对应的元素.

(1)表中属于ds区的元素是 (填编号).
(2)元素②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨.有关该化合物分子的说法不正确的是 .
A.分子中含极性共价键 B.含有2个σ键和2个π键
C.属于非极性分子 D.该化合物分子中,②原子采用sp2杂化
(3)根据上述表格中的十种元素填空:
Ⅰ、金属性最强的主族元素的电子排布式为 ;
Ⅱ、⑤、⑥、⑦的离子半径由小到大的顺序是 (填化学式)
Ⅲ、⑥、⑦两种元素的最高价氧化物对应的水化物的酸性由大到小的顺序是 (填化学式)
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为 ;该元素与元素①形成的分子X的空间构型为 .

(1)表中属于ds区的元素是
(2)元素②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨.有关该化合物分子的说法不正确的是
A.分子中含极性共价键 B.含有2个σ键和2个π键
C.属于非极性分子 D.该化合物分子中,②原子采用sp2杂化
(3)根据上述表格中的十种元素填空:
Ⅰ、金属性最强的主族元素的电子排布式为
Ⅱ、⑤、⑥、⑦的离子半径由小到大的顺序是
Ⅲ、⑥、⑦两种元素的最高价氧化物对应的水化物的酸性由大到小的顺序是
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为
分析:由元素在周期表中的位置可知,①为H,②为C,③为O,④为Mg,⑤为Al,⑥为S,⑦为Cl,⑧为Ca,⑨为Ni,⑩为Cu,
(1)以上元素只有Cu为ds区元素;
(2)②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨,该化合物为CO2,为含极性键的非极性分子,C原子为sp杂化,双键中含1个σ键和1个π键;
(3)I、以上元素,金属性最强的为Ca,原子序数为20;
II、离子的电子层越多,半径越大,具有相同电子层结构的离子,原子序数大的离子半径小;
Ⅲ、⑥、⑦的非金属性为Cl>S,非金属性越强,元素的最高价氧化物对应的水化物的酸性越强;
(4)元素的特征电子排布式为nsnnpn+1,s最多有2个电子,所以n=2,即电子排布式为1s22s22p3,该元素为N元素,核外最外层电子的孤对电子数为1,单电子为3,与元素①形成的分子X为NH3,为三角锥型.
(1)以上元素只有Cu为ds区元素;
(2)②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨,该化合物为CO2,为含极性键的非极性分子,C原子为sp杂化,双键中含1个σ键和1个π键;
(3)I、以上元素,金属性最强的为Ca,原子序数为20;
II、离子的电子层越多,半径越大,具有相同电子层结构的离子,原子序数大的离子半径小;
Ⅲ、⑥、⑦的非金属性为Cl>S,非金属性越强,元素的最高价氧化物对应的水化物的酸性越强;
(4)元素的特征电子排布式为nsnnpn+1,s最多有2个电子,所以n=2,即电子排布式为1s22s22p3,该元素为N元素,核外最外层电子的孤对电子数为1,单电子为3,与元素①形成的分子X为NH3,为三角锥型.
解答:解:由元素在周期表中的位置可知,①为H,②为C,③为O,④为Mg,⑤为Al,⑥为S,⑦为Cl,⑧为Ca,⑨为Ni,⑩为Cu,
(1)元素周期表中位于ds区的元素为第ⅠB、ⅡB族,以上元素只有Cu为ds区元素,故答案为:⑩;
(2)②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨,该化合物为CO2,
A.分子中含C、O之间的极性共价键,故A正确;
B.结构式为O=C=O,含有2个σ键和2个π键,故B正确;
C.结构对称,正负电荷中心重合,为含极性键的非极性分子,故C正确;
D.该化合物分子为直线型,②原子采用sp杂化,故D错误;
故答案为:D;
(3)I、以上元素,金属性最强的为Ca,原子序数为20,其电子排布式为1s22s22p63s23p64s2,故答案为:1s22s22p63s23p64s2;
II、离子的电子层越多,半径越大,具有相同电子层结构的离子,原子序数大的离子半径小,所以离子半径由小到大的顺序为Al3+<Cl-<S2-,
故答案为:Al3+<Cl-<S2-;
Ⅲ、⑥、⑦的非金属性为Cl>S,非金属性越强,元素的最高价氧化物对应的水化物的酸性越强,所以酸性为HClO4>H2SO4,故答案为:HClO4>H2SO4;
(4)元素的特征电子排布式为nsnnpn+1,s最多有2个电子,所以n=2,即电子排布式为1s22s22p3,该元素为N元素,最外层为第2层,2s电子为孤对电子,孤对电子数为1,2p电子均为单电子,则单电子为3,与元素①形成的分子X为NH3,N原子为sp3杂化,空间构型为三角锥型,故答案为:1;三角锥型.
(1)元素周期表中位于ds区的元素为第ⅠB、ⅡB族,以上元素只有Cu为ds区元素,故答案为:⑩;
(2)②与③形成的一种化合物是重要的化工原料,该化合物可用于人工降雨,该化合物为CO2,
A.分子中含C、O之间的极性共价键,故A正确;
B.结构式为O=C=O,含有2个σ键和2个π键,故B正确;
C.结构对称,正负电荷中心重合,为含极性键的非极性分子,故C正确;
D.该化合物分子为直线型,②原子采用sp杂化,故D错误;
故答案为:D;
(3)I、以上元素,金属性最强的为Ca,原子序数为20,其电子排布式为1s22s22p63s23p64s2,故答案为:1s22s22p63s23p64s2;
II、离子的电子层越多,半径越大,具有相同电子层结构的离子,原子序数大的离子半径小,所以离子半径由小到大的顺序为Al3+<Cl-<S2-,
故答案为:Al3+<Cl-<S2-;
Ⅲ、⑥、⑦的非金属性为Cl>S,非金属性越强,元素的最高价氧化物对应的水化物的酸性越强,所以酸性为HClO4>H2SO4,故答案为:HClO4>H2SO4;
(4)元素的特征电子排布式为nsnnpn+1,s最多有2个电子,所以n=2,即电子排布式为1s22s22p3,该元素为N元素,最外层为第2层,2s电子为孤对电子,孤对电子数为1,2p电子均为单电子,则单电子为3,与元素①形成的分子X为NH3,N原子为sp3杂化,空间构型为三角锥型,故答案为:1;三角锥型.
点评:本题考查位置、结构、性质的应用,涉及元素周期表中元素的分区、元素周期表中元素的位置、电子排布式、分子构型、非金属性比较等,综合性较强,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目