题目内容
11.下列物质能跟镁反应并生成氢气的是( )| A. | 常温下在蒸馏水中 | B. | 氢氧化钠溶液 | ||
| C. | 氯化铵溶液 | D. | 碳酸钠溶液 |
分析 金属镁的金属强较强,可以和酸或是水解显酸性的盐溶液反应生成氢气.
解答 解:A、常温下,蒸馏水和金属镁不反应,故A错误;
B、氢氧化钠溶液显碱性,和金属镁不反应,故B错误;
C、氯化铵中的铵根离子水解显酸性,可以和金属镁反应产生氢气,故C正确;
D、碳酸钠中的碳酸根离子水解显碱性,不能和金属镁反应,故D错误.
故选C.
点评 本题考查学生金属镁的化学性质,由于盐中某些离子的水解导致盐溶液有的不再显中性是解此题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列四种X溶液,分别放入盛有10mL 2mol•L -1HCl的烧杯中,加水稀释至50mL,X和HCl进行反应,其中反应速率最大的是( )
| A. | 20mL3mol•L -1X的溶液 | B. | 20mL2mol•L -1X的溶液 | ||
| C. | 10mL4mol•L -1X的溶液 | D. | 10mL2mol•L -1X的溶液 |
2.某电化学装置工作原理如图,下列有关说法正确的是( )
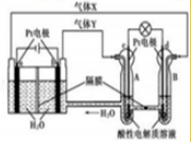

| A. | 气体X为O2 | |
| B. | c电极为负极,发生的电极反应式为H2-2e-=2H+ | |
| C. | 一段时间后A处PH降低 | |
| D. | 当有0.4mol电子转移时,在B极上生成标准状况下气体2.24L |
19.下列说法中正确的是( )
| A. | 最外层电子数相同的元素一定属于同一族 | |
| B. | 同周期元素的电子层数相同 | |
| C. | 非金属元素的最外层电子数都≧4 | |
| D. | 元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 |
6.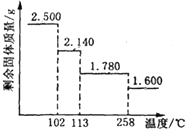 胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )
胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )
 胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )
胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图.以下说法正确的是 ( )| A. | 晶体从常温升至105℃的过程中只有氢键断裂 | |
| B. | 受热过程中,胆矾晶体中形成配位键的4个水分子同时失去 | |
| C. | 120℃时,剩余固体的化学式是CuSO4•H2O | |
| D. | 按胆矾晶体失水时所克服的作用力大小不同,晶体中的水分子所处化学环境可以分为3种 |
3.某温度下,甲溶液的pH是乙溶液的两倍,则甲溶液中H+的浓度与乙溶液中H+的浓度的关系是( )
| A. | 2:1 | B. | 100:1 | C. | 1:100 | D. | 无法确定 |
20.NA代表阿伏加德罗常数,以下说法正确的是( )
| A. | 12lg CCl2F2所含的氯原子数为2NA | |
| B. | 常温常压下l mol NO2气体与水反应生成NA个NO3一离子 | |
| C. | 氯化氢气体的摩尔质量等于NA个氯原子和NA个氢原子的质量之和 | |
| D. | 124g Na2O溶于水后所得溶液中含有O2-离子数为2NA |



 .
.