题目内容
向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图一所示.图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知t3~t4阶段使用了催化剂;图一中t0~t1阶段c(B)未画出.
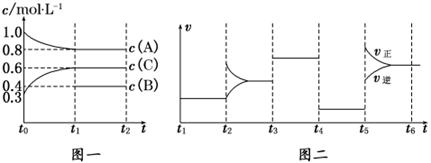
(1)若t1=15 min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=_______________.
(2)t4~t5阶段改变的条件为_______________,B的起始物质的量为_______________.
各阶段平衡时对应的平衡常数如下表所示:
|
t1~t2 |
t2~t3 |
t3~t4 |
t4~t5 |
t5~t6 |
|
K1 |
K2 |
K3 |
K4 |
K5 |
则K1=_______________ (保留两位小数),K1、K2、K3、K4、K5之间的关系为____ (用“>”、“<”或“=”连接).
(1)0.02 mol/(L·min) (2)减小压强 1.0 mol 0.84 K1=K2=K3=K4<K5
【解析】
试题分析:(1)t1=15 min,C的浓度增加了0.6mol/L-0.3mol/L=0.3mol/L,注意t0~t1阶段以C浓度变化表示的反应速率为v(C)=0.3mol/L÷15min=0.02 mol/(L·min)。
(2)根据图像2可知,在t4~t5和t3~t4阶段,反应速率均同时增大或同时减小,但平衡都不移动。阶段在可知,四个阶段都各改变一种不同的条件,这说明反应前后该反应一定是体积不变的可逆反应。根据图像1可知,平衡时A减少了0.2mol/L,所以根据浓度的变化量之比是相应的化学计量数之比可知,B一定是反应物,且B的浓度减少了0.1mol/L,即该反应的方程式是2A+B 3C。所以起始时B的浓度是0.5mol/L。容器的体积是2mol÷1mol/L=2L,所以B物质的起始物质的量是1mol。t4~t5阶段改变的条件为降低压强。
3C。所以起始时B的浓度是0.5mol/L。容器的体积是2mol÷1mol/L=2L,所以B物质的起始物质的量是1mol。t4~t5阶段改变的条件为降低压强。
(3)根据图像1可知,K1=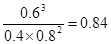 。根据图像2可知,t5时改变的条件是升高温度,正反应速率大于逆反应速率,即正方应是吸热反应,所以平衡常数增大,则K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。根据图像2可知,t5时改变的条件是升高温度,正反应速率大于逆反应速率,即正方应是吸热反应,所以平衡常数增大,则K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
考点:考查反应速率、平衡常数的有关计算以及外界条件对平衡状态的影响
点评:该题是中等难度的试题,试题基础性强,侧重对学生基础知识的巩固和训练。该题的关键是明确反应速率和平衡常数的含义以及影响因素,然后图像和方程式灵活运用即可。有利于培养学生的逻辑推理能力,提高学生分析、归纳、总结问题的能力。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
 2NH3(g),则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”) ;向另一电极通入N2,该电极的反应式为__________________________。
2NH3(g),则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”) ;向另一电极通入N2,该电极的反应式为__________________________。 4NH3(g)+3O2(g) △H=Q。
4NH3(g)+3O2(g) △H=Q。 与反应温度T的关系曲线如图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
