题目内容
下列根据实验操作和现象所得出的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH | 前者的pH比后者的大 | 元素非金属性:S>C |
| B | SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | SO2具有漂白性 |
| C | 溴乙烷与NaOH溶液共热后,加稀硝酸酸化的AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| D | 向等浓度的KBr、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgBr)>Ksp(AgI) |
- A.A
- B.B
- C.C
- D.D
AB
分析:A.Na2CO3的水解程度大,应利用最高价氧化物水化物的酸性比较非金属性比较;
B.SO2通入酸性高锰酸钾溶液,发生氧化还原反应;
C.溴乙烷与NaOH溶液共热后,发生水解生成NaBr,加稀硝酸酸化的AgNO3溶液,反应生成AgBr;
D.溶度积小的物质先转化为沉淀.
解答:A.测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,Na2CO3的水解程度大,前者的pH比后者的大,不能比较非金属性,应利用最高价氧化物水化物的酸性比较非金属性比较,故A错误;
B.SO2通入酸性高锰酸钾溶液,发生氧化还原反应,溶液褪色,说明二氧化硫具有还原性,故B错误;
C.溴乙烷与NaOH溶液共热后,发生水解生成NaBr,加稀硝酸酸化的AgNO3溶液,反应生成AgBr,观察到出现淡黄色沉淀,故C正确;
D.向等浓度的KBr、KI混合液中滴加AgNO3溶液,溶度积小的物质先转化为沉淀,先出现黄色沉淀,说明Ksp(AgBr)>Ksp(AgI),故D正确;
故选AB.
点评:本题考查化学实验方案的评价,涉及盐类水解、pH、氧化还原反应、卤代烃水解、沉淀的生成等,注重基础知识的考查,题目难度不大.
分析:A.Na2CO3的水解程度大,应利用最高价氧化物水化物的酸性比较非金属性比较;
B.SO2通入酸性高锰酸钾溶液,发生氧化还原反应;
C.溴乙烷与NaOH溶液共热后,发生水解生成NaBr,加稀硝酸酸化的AgNO3溶液,反应生成AgBr;
D.溶度积小的物质先转化为沉淀.
解答:A.测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,Na2CO3的水解程度大,前者的pH比后者的大,不能比较非金属性,应利用最高价氧化物水化物的酸性比较非金属性比较,故A错误;
B.SO2通入酸性高锰酸钾溶液,发生氧化还原反应,溶液褪色,说明二氧化硫具有还原性,故B错误;
C.溴乙烷与NaOH溶液共热后,发生水解生成NaBr,加稀硝酸酸化的AgNO3溶液,反应生成AgBr,观察到出现淡黄色沉淀,故C正确;
D.向等浓度的KBr、KI混合液中滴加AgNO3溶液,溶度积小的物质先转化为沉淀,先出现黄色沉淀,说明Ksp(AgBr)>Ksp(AgI),故D正确;
故选AB.
点评:本题考查化学实验方案的评价,涉及盐类水解、pH、氧化还原反应、卤代烃水解、沉淀的生成等,注重基础知识的考查,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
阿司匹林是一种历史悠久的解热镇痛药,学名为乙酰水杨酸,结构简式为 。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
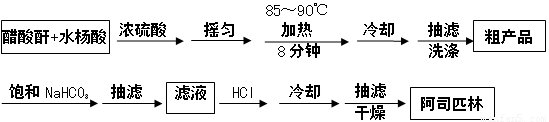
已知:1、乙酰水杨酸是白色晶体,易溶于乙醇、乙醚,在128~135℃易分解。
2、主要试剂和产品的其它物理常数
|
名称 |
相对分子质量 |
熔点或沸点(℃) |
水溶性 |
|
水杨酸 |
132 |
158(熔点) |
微溶 |
|
醋酸酐 |
102 |
139.4(沸点) |
与水反应 |
|
乙酰水杨酸 |
180 |
135(熔点) |
微溶 |
请根据以上信息回答下列问题:
(1)写出水杨酸与醋酸酐制备阿司匹林的化学方程式 。
(2)制备阿司匹林主反应时,仪器必须干燥的原因是 。
(3)合成阿司匹林主反应时,最合适的加热方法是 ,除酒精灯外,该加热装置还需要的玻璃仪器有 。
(4)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤(即减压过滤),结合提纯流程回答加饱和NaHCO3溶液的目的是 。
(5)最终所得产品可能仍含有少量水杨酸,检验含有水杨酸的操作和现象是
。



