题目内容
【题目】某同学用如图装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究,回答下列问题。
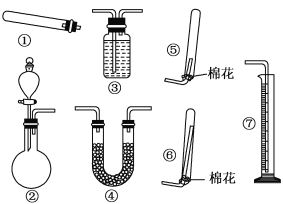
(1)若用装置①制取NH3,其反应的化学方程式为_________;若要测定生成的NH3的体积,则必须选择的装置是________(填装置序号)。
(2)若用装置②制取并收集干燥的NH3,烧瓶内装的试剂可以是______,收集装置应选择________(填装置序号)。
(3)下列气体中,可用碱石灰干燥的是________(填字母)。
A.H2 B.Cl2 C.SO2 D.NH3
【答案】2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O ③⑦ CaO或NaOH或碱石灰 ⑥ AD
2NH3↑+CaCl2+2H2O ③⑦ CaO或NaOH或碱石灰 ⑥ AD
【解析】
(1)装置①适用于固体加热制气体,实验室中可加热氯化铵和氢氧化钙固体混合物制取氨气,化学方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;氨气极易溶于水,无法排水收集,但可以在装置③盛放不能溶解氨气的液体,将生成的氨气短进长出导入到装置③中,将装置中液体排出到量筒中,通过液体的体积确定生成的氨气体积,所以选③⑦;
2NH3↑+CaCl2+2H2O;氨气极易溶于水,无法排水收集,但可以在装置③盛放不能溶解氨气的液体,将生成的氨气短进长出导入到装置③中,将装置中液体排出到量筒中,通过液体的体积确定生成的氨气体积,所以选③⑦;
(2)装置②适用于固体与液体常温下制气体,氨气为碱性气体,可用CaO、NaOH、碱石灰等碱性物质与浓氨水作用制氨气;氨气极易溶于水,氨气密度比空气小,可用向下排空气法收集,将导管插入到倒置试管底部,所以选用⑥;
(3)氢气和氨气均不与碱石灰反应,可以用碱石灰干燥,氯气、SO2会和碱石灰发生反应,不能用碱石灰干燥,所以选AD。

【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=![]() mol/L
mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)