题目内容
发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,已知:N2(g)+O2(g)=2NO2(g)△H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol
试写出N2H4与 NO2反应的热化学方程式 .
【答案】分析:依据热化学方程式的意义和盖斯定律的内容通过合并计算得到热化学方程式.
解答:解:①N2(g)+O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol
依据盖斯定律:②×2-①得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
点评:本题考查了热化学方程式的书写方法和盖斯定律的计算应用,题目较简单.
解答:解:①N2(g)+O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol
依据盖斯定律:②×2-①得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
点评:本题考查了热化学方程式的书写方法和盖斯定律的计算应用,题目较简单.

练习册系列答案
相关题目
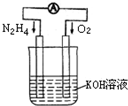 运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.