题目内容
铜锌原电池工作时,下列叙述正确的是
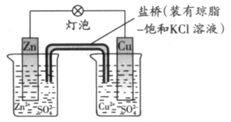
- A.正极反应为:Zn—2e-=Zn2+
- B.B、在外电路中,电子从铜片流向锌片
- C.电池反应为:Zn+Cu2+=Zn2+ +Cu
- D.盐桥中的K+移向ZnSO4溶液
C
试题分析:A:锌极发生氧化反应,是负极;B:锌极失去电子被氧化,铜极得到电子被还原,在外电路电子是从锌极流向铜极;D:盐桥中的溶液是电解质溶液,由于锌极失去电子成为Zn2+
进入溶液,使ZnSO4溶液带正电,所以盐桥中的Cl-会移向ZnSO4溶液,使溶液保持电中性,氧化还原反应得以继续进行,故D错。
考点:原电池,盐桥的作用
点评:本题考查原电池的工作原理,难度不大,注意基础知识的积累。
试题分析:A:锌极发生氧化反应,是负极;B:锌极失去电子被氧化,铜极得到电子被还原,在外电路电子是从锌极流向铜极;D:盐桥中的溶液是电解质溶液,由于锌极失去电子成为Zn2+
进入溶液,使ZnSO4溶液带正电,所以盐桥中的Cl-会移向ZnSO4溶液,使溶液保持电中性,氧化还原反应得以继续进行,故D错。
考点:原电池,盐桥的作用
点评:本题考查原电池的工作原理,难度不大,注意基础知识的积累。

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目


