题目内容
下列离子方程式正确的是( )
| A、FeCl3 溶液与铁反应:Fe+Fe3+═2Fe2+ |
| B、向Ca(HCO3)2溶液中加入足量NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、铝粉溶于NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| D、金属钠跟水反应Na+2H2O═Na++OH-+H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷、电子不守恒;
B.反应生成碳酸钙、碳酸钠和水;
C.反应生成偏铝酸钠和氢气,遵循电子、电荷守恒;
D.电子、原子不守恒.
B.反应生成碳酸钙、碳酸钠和水;
C.反应生成偏铝酸钠和氢气,遵循电子、电荷守恒;
D.电子、原子不守恒.
解答:
解:A.FeCl3溶液与铁反应的离子反应为Fe+2Fe3+═3Fe2+,故A错误;
B.向Ca(HCO3)2溶液中加入足量NaOH溶液的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故B错误;
C.铝粉溶于NaOH溶液中的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,故C正确;
D.金属钠跟水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故D错误;
故选C.
B.向Ca(HCO3)2溶液中加入足量NaOH溶液的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故B错误;
C.铝粉溶于NaOH溶液中的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,故C正确;
D.金属钠跟水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故D错误;
故选C.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意离子反应中保留化学式的物质及电子、电荷守恒的应用,题目难度不大.

练习册系列答案
相关题目
 某农民偶然发现他的一头小牛食用腐败草料后,在受外伤时血液不会凝固,流血不止.化学家由此得到启发,从腐败草料中提取出结构简式如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小牛食用腐败草料后,在受外伤时血液不会凝固,流血不止.化学家由此得到启发,从腐败草料中提取出结构简式如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A、分子式为C19H12O6,有望将它发展制得一种抗凝血药 |
| B、可用来制备致命性出血型的杀鼠药 |
| C、所有碳原子不可能在同一平面 |
| D、可发生水解、加成、氧化反应 |
下列事实与氢键无关的是( )
| A、卤化氢中,以HF沸点最高 |
| B、水结成冰体积膨胀 |
| C、邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 |
| D、水加热到很高的温度都难以分解 |
下列叙述正确的是( )
| A、在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B、没有单质参加的反应一定不是氧化还原反应 |
| C、置换反应一定是氧化还原反应 |
| D、较难失去电子的原子,容易得到电子 |
仅能在水溶液中导电的非电解质是( )
| A、SO3 |
| B、NH4Cl |
| C、Cl 2 |
| D、Na2CO3 |
下列变化属于物理变化的是( )
| A、电解质溶液的导电 |
| B、石油裂解 |
| C、煤的干馏 |
| D、四氯化碳萃取碘水中的I2 |
某固态化合物X不导电,但其熔化或溶于水时都能完全电离.下列关于物质X的说法中,正确的是( )
| A、X为非电解质 |
| B、X是弱电解质 |
| C、X是强电解质 |
| D、X为易溶性盐 |
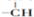 和一个
和一个 .则该有机物可能的结构有(不考虑立体异构)( )
.则该有机物可能的结构有(不考虑立体异构)( ) 在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表: