题目内容
13.已知六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E和F同周期.常温下单质A与E的状态不同,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料,则下列推断正确的是( )| A. | 由A、C两种元素的原子可形成10电子的分子 | |
| B. | F与D形成的稳定化合物能用来制作信息材料,不与任何酸反应 | |
| C. | 原子半径的大小顺序:r(E)>r(F)>r(D)>r(C) | |
| D. | 某些元素气态氢化物稳定性由强到弱的顺序:D>C>F>B |
分析 六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F是Si元素;B和F同一主族,且都是短周期元素,所以B是C元素;E和F同一周期,且E的原子序数小于F,A与E同主族,常温下单质A与E的状态不同,则A是H元素、E是Na元素;D的核电荷数是B的最外层电子数的2倍,B的原子最外层电子数是4,则D是O元素,C原子序数大于B而小于D,所以C是N元素,再结合元素周期律知识解答.
解答 解:六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F是Si元素,B和F同一主族,且都是短周期元素,所以B是C元素;E和F同一周期,且E的原子序数小于F,A与E同主族,常温下单质A与E的状态不同,则A是H元素、E是Na元素;D的核电荷数是B的最外层电子数的2倍,B的原子最外层电子数是4,则D是O元素,C原子序数大于B而小于D,所以C是N元素,
A.A是H元素、C是N元素,A、C两种元素可组成含有10个电子的NH3,故A正确;
B.F是Si元素、D是O元素,二者形成的化合物SiO2能溶于HF,故B错误;
C.原子电子层数越多其原子半径越大,同一周期元素,其原子半径随着原子序数增大而减小,所以原子半径大小顺序是Na>Si>N>O,即r(E)>r(F)>r(C)>r(D),故C错误;
D.同一周期元素,元素非金属性随着原子序数增大而增强,同一主族元素,非金属元素非金属性随着原子序数增大而减弱,所以非金属性D>C>B>F,非金属性越强,气态氢化物的稳定性越强,则气态氢化物稳定性由强到弱的顺序为:D>C>B>F,故D错误;
故选A.
点评 本题考查原子结构和元素周期律的关系,正确推断元素是解本题关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及逻辑推理能力.

①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;
②用NaOH溶液除去苯中的少量苯酚;
③用饱和NaHCO3溶液除去CO2中的少量SO2;
④用加热方法提取NH4Cl固体中混有少量碘;
⑤用醋酸和澄清石灰水验证蛋壳中含有碳酸盐;
⑥用浓溴水除去苯中少量苯酚;
⑦用碘酒验证汽油中含有不饱和烃;
⑧用溴水除去甲烷中混有的少量乙烯.
| A. | ①②⑥⑦⑧ | B. | ①③⑤⑥⑦ | C. | ②③⑤⑦⑧ | D. | ②③④⑤⑦ |
| A. | O2和O3的相互转化是物理变化 | |
| B. | O2和O3互为同素异形 | |
| C. | 等物质的量的O2和O3含有的质子数不相同 | |
| D. | 在相同的温度与压强下,等体积的O2和O3含有相同的分子数 |
| A. | 在共价化合物中也可能含有离子键 | |
| B. | 非金属之间形成的化学键不一定是共价键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 含有离子键的化合物一定是离子化合物 |
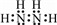 .
. ,N采用sp3杂化方式,粒子空间构型为V形.
,N采用sp3杂化方式,粒子空间构型为V形.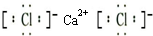 .
.