题目内容
9.下列有关实验的说法正确的是( )| A. | 某学生用pH试纸测新制氯水的pH值,先变红后褪色,是因为Cl2有强氧化性 | |
| B. | 容量瓶、分液漏斗、滴定管在使用前要检查是否漏水 | |
| C. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 | |
| D. | 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化 |
分析 A.氯气没有漂白性,次氯酸有漂白性;
B.根据带有旋塞和瓶塞的仪器,一般在使用前需要检查是否漏水;
C.瓷坩埚中含有二氧化硅,在加热条件下能与氢氧化钠反应;
D.铜和浓硫酸在加热条件下发生氧化还原反应.
解答 解:A.氯气和水反应生成盐酸和次氯酸,溶液呈酸性,所以用PH试纸测溶液的PH值时试纸变红,次氯酸有漂白性,能使红色试纸褪色,故A错误;
B.分液漏斗、容量瓶、滴定管是带有旋塞和瓶塞的仪器,使用前需要检查是否漏水,故B正确;
C.瓷坩埚中含有二氧化硅,在加热条件下能与氢氧化钠反应而导致坩埚炸裂,故C错误;
D.铜和浓硫酸在常温下不反应,加热条件下发生氧化还原反应,故D错误.
故选:B.
点评 本题为综合题,考查了氯水、二氧化硅、浓硫酸的性质,常见化学仪器的使用方法,侧重考查学生对基础知识掌握,题目难度不大.

练习册系列答案
相关题目
17.向a g锌和铜的混合物中加入适量的稀硝酸,恰好完全反应,假定生成气体只有NO,其标准状况下的体积为b L.向反应后的溶液中加入c mol•L-1氢氧化钠溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为d g.再将得到的沉淀灼烧至质量不再改变为止,得到固体e g.则下列关系不正确的是( )
| A. | c=$\frac{3b}{0.0224V}$ | B. | e=a+$\frac{8cV}{1000}$ | C. | d=a+$\frac{17cV}{1000}$ | D. | $\frac{82a}{65}$<e<$\frac{5a}{4}$ |
3.目前我省不少城市居民所使用的燃料主要是管道煤气,有的地方已经开始使用天然气作为民用燃料.管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4.它们的燃烧反应如下:
2CO+O2$\stackrel{点燃}{→}$2CO2 2H2+O2$\stackrel{点燃}{→}$2H2O CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气.因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是增大进风口(填增大或减小),如不作改进可能产生的不良结果是天然气不能充分燃烧,可能生成有毒的CO
管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是丁烷遇冷凝结为液体使管道内气流不畅.
2CO+O2$\stackrel{点燃}{→}$2CO2 2H2+O2$\stackrel{点燃}{→}$2H2O CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气.因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是增大进风口(填增大或减小),如不作改进可能产生的不良结果是天然气不能充分燃烧,可能生成有毒的CO
管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质见下表:
| 乙烷 | 丙烷 | 丁烷 | |
| 熔点(℃) | -183.3 | -189.7 | -138.4 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 |
10. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
(1)①写出工业合成氨的化学方程式N2+3H2$?_{高温高压}^{催化剂}$2NH3.
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a molH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
②理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a molH2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
7.下列叙述不正确的是( )
| A. | 乙烯、油脂、天然橡胶和蛋白质分子中均含有双键 | |
| B. | 相同物质的量的甲基、羟基或氨基所含的电子数目相同 | |
| C. | 常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数不为定值 | |
| D. | 利用红外光谱仪记录的红外光谱图可以初步推测有机化合物中官能团的类别 |

 .
.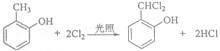 .
. .
. 既可发生酯化反应生成香豆素,可发生加聚反应.该物质加聚产物的结构简式为
既可发生酯化反应生成香豆素,可发生加聚反应.该物质加聚产物的结构简式为 .
.


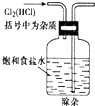
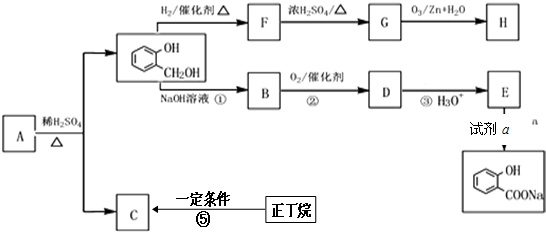
 ,由F到G的反应类型为消去反应.
,由F到G的反应类型为消去反应.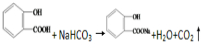 .
.
 的反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:取少量反应后的溶液于试管中,加入氯化铁溶液,若溶液变紫色,则反应不完全,反应物有剩余,反之则完全反应.
的反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:取少量反应后的溶液于试管中,加入氯化铁溶液,若溶液变紫色,则反应不完全,反应物有剩余,反之则完全反应.