题目内容
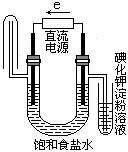
用石墨电极电解1L含硝酸铜和氯化钠各 0.1mol的混合溶液,当阳极上生成的气体在标准状况下体积为2.24L时,假设溶液的体积不变,下列说法正确的是:(标准状况下)( )
分析:离子放电顺序为Cu2+>H+>Na+,Cl->OH->NO3-,阳极依次发生:2Cl--2e-═Cl2↑,4OH--4e-═O2↑+2H2O;阴极依次发生Cu2++2e-═Cu,2H++2e-═H2↑,阳极生成气体的物质的量为
=0.1mol,说明阳极Cl-全被放电,且部分OH-被氧化生成O2,以此解答该题.
| 2.24L |
| 22.4L/mol |
解答:解:离子放电顺序为Cu2+>H+>Na+,Cl->OH->NO3-,阳极依次发生:2Cl--2e-═Cl2↑,4OH--4e-═O2↑+2H2O;阴极依次发生Cu2++2e-═Cu,2H++2e-═H2↑,阳极生成气体的物质的量为
=0.1mol,
n(NaCl)=0.1mol,
则阳极Cl-全被放电,生成氯气0.05mol,
还应生成0.05molO2,
则阳极共失去电子为0.05mol×2+0.05mol×4=0.3mol,
因n(Cu2+)=0.1mol,全部放电得到0.2mol电子,且阴极增重6.4g,
则阴极还应发生2H++2e-=H2↑,得到0.1mol电子,生成0.05molH2,
反应后溶液为硝酸和硝酸钠的混合溶液,呈酸性,
故选:C.
| 2.24L |
| 22.4L/mol |
n(NaCl)=0.1mol,
则阳极Cl-全被放电,生成氯气0.05mol,
还应生成0.05molO2,
则阳极共失去电子为0.05mol×2+0.05mol×4=0.3mol,
因n(Cu2+)=0.1mol,全部放电得到0.2mol电子,且阴极增重6.4g,
则阴极还应发生2H++2e-=H2↑,得到0.1mol电子,生成0.05molH2,
反应后溶液为硝酸和硝酸钠的混合溶液,呈酸性,
故选:C.
点评:本题考查电解原理,侧重于学生的分析能力和计算能力的考查,为高考高频考点,难度中等,注意把握离子的放电顺序,为解答该题的关键.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题: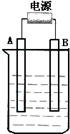 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题: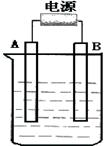







 B、
B、
 D、
D、