题目内容
3.碳、氮及其化合物是同学们经常能接触到的重要物质,是科学研究的重要对象.(1)实验室制取乙炔的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑.
(2)H2NCOONH4是工业合成尿素的中间产物,该反应的能量变化如图A所示.用CO2和氨气合成尿素的热化学方程式为2NH3(l)+CO2(g)=H2O(l)+H2NCONH2 (l)△H=-134.0kJ•mol-1.

(3)合理利用CO2、CH4,抑制温室效应成为科学研究的新热点.一种以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸(△H<0).在不同温度下催化剂的催化效率与乙酸的生成速率分别如图B所示.250~300℃时,温度升高而乙酸的生成速率降低的原因是250℃,催化剂的催化效率最好,之后催化剂的催化效率急剧降低.250℃和400℃时乙酸的生成速率几乎相等,实际生产中应选择的温度为250℃.
(4)T℃时,将等物质的量的NO和CO充入体积为2L的 密闭容器中发生反应2NO+2CO?2CO2+N2.保持温度和体积不变,反应过程中NO的物质的量随时间的变化如图C所示.
①平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将向右(填“向左”、“向右”或“不”)移动.
②图中a、b分别表示在一定温度下,使用相同质量、不同表面积的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是b(填“a”或“b”).
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是增大CO的物质的量浓度(或增大压强)(任答一条即可).
(5)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,可用电解原理将溶液中的氨氮物质完全氧化除去.该过程分为两步:第一步:电解产生氯气;第二步:利用氯气将氨氮物质氧化为N2.
①第二步反应的化学方程式为3Cl2+2NH3=N2+6HCl.
②若垃圾渗滤液中氨氮物质的质量分数为0.034%,理论上用电解法净化It该污水,电路中转移的电子数为60NA.
分析 (1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔;
(2)根据盖斯定律及已知热化学方程式写出目标热化学方程式;
(3)由图象得,250℃,催化剂的催化效率最好,之后催化剂的催化效率急剧降低,据此进行分析;据温度低,能耗低,节约经济成本;
(4)①根据Qc与k的相对大小分析;
②催化剂表面积较大,反应速率快,达到平衡所用时间短;
③由图象可知,NO的浓度减小,平衡向正方向移动;
(5)①第二步氧化剂氯气氧化氨氮物质即氨气生成N2的过程,发生的反应为:3Cl2+2NH3=N2+6HCl;
②3Cl2+2NH3=N2+6HCl~6mole-,据此方程式进行计算.
解答 解:(1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(2)已知①2NH3(l)+CO2(g)═H2NCOONH4(氨基甲酸铵)(l)△H1=-272.0kJ•mol-1
②H2NCOONH4(l)═H2O(l)+H2NCONH2(l)△H2=+138.0kJ•mol-1,
根据盖斯定律,①+②可得:2NH3(l)+CO2(g)═H2O(l)+H2NCONH2 (l),△H=-272.0kJ•mol-1+138.0kJ•mol-1=-134.0kJ•mol-1,
故答案为:2NH3(l)+CO2(g)=H2O(l)+H2NCONH2 (l)△H=-134.0kJ•mol-1;
(3)由图象得,250~300℃时,温度升高而乙酸的生成速率降低的原因是250℃,催化剂的催化效率最好,之后催化剂的催化效率急剧降低;250℃和400℃时乙酸的生成速率几乎相等,由于温度低,能耗低,节约经济成本,故实际生产中应选择的温度为250℃,
故答案为:250℃,催化剂的催化效率最好,之后催化剂的催化效率急剧降低;250;
(4)①起始时,NO为0.4mol,平衡时NO为0.2mol,
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2
起始物质的量:0.4mol 0.4mol 0 0
转化的物质量:0.2mol 0.2mol 0.2mol 0.1mol
平衡物质的量:0.2mol 0.2mol 0.2mol 0.1mol
则平衡时的浓度:c(NO)=0.1mol/L,c(CO)=0.1mol/L,c(CO2)=0.1mol/L,c(N2)=0.05mol/L,
该稳定性该反应的平衡常数K=$\frac{0.{1}^{2}×0.05}{0.{1}^{2}×0.{1}^{2}}$=5;
平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,则c(CO)=0.5mol/L,c(N2)=0.45mol/L,
此时的浓度商Qc=$\frac{0.{1}^{2}×0.45}{0.{1}^{2}×0.{5}^{2}}$=1.8<k,则平衡将向右移动,
故答案为:向右;
②催化剂表面积较大,反应速率快,达到平衡所用时间短,由图可知,b曲线代表的条件下反应速率快,所以b的催化剂的表面积大;
故答案为:b;
③由图象可知,NO的浓度减小,平衡向正方向移动,所以改变的条件为增加CO的物质的量浓度或增大压强;
故答案为:增大CO的物质的量浓度(或增大压强);
(5)①第二步氧化剂氯气氧化氨氮物质即氨气生成N2的过程,发生的反应为:3Cl2+2NH3=N2+6HCl,
故答案为:3Cl2+2NH3=N2+6HCl;
②m(NH3)=0.034%×1t=340g,
3Cl2+2NH3=N2+6HCl~6mole-
34 6
340 60,则n(e-)=60mol,故N(e-)=60NA,
故答案为:60NA.
点评 本题考查较为综合,涉及化学平衡的计算、反应热与焓变、电子转移的计算及化学方程式的书写,题目难度中等,明确化学平衡及其影响为解答关键,注意掌握三段式在化学平衡计算中的应用,试题培养了学生的分析、理解能力及化学计算能力.

 科学实验活动册系列答案
科学实验活动册系列答案| A. | 通过电解熔融CD3可以制备C单质 | |
| B. | A和B可以形成气体,其分子一定为正四面体结构 | |
| C. | C的氢氧化物可以溶于D的最高价氧化物的水化物 | |
| D. | A2B2O4在水中可电离出阳离子和阴离子,所以A2B2O4中存在离子键 |
| A. | NaOH、FeSO4在空气中放置变质 | B. | 氯水、AgI密封保存在棕色试剂瓶中 | ||
| C. | SO2使品红和酸性KMnO4溶液褪色 | D. | 常温下浓硝酸不能溶解Al和Au(金) |
 甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁元素主要以单质的形态存在于自然界中 |
 已知:
已知:①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H1=-905.5kJ•molˉ1
②N2(g)+O2(g)?2NO(g)△H2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下:
③4NH3(g)+4NO(g)+O2(g)?4N2(g)+6H2O(g)△H3=-1625.5 kJ•molˉ1下列说法正确的是( )
| A. | 反应①使用催化剂,△H1减小 | |
| B. | 反应②生成物总能量低于反应物总能量 | |
| C. | 反应③一定能自发进行 | |
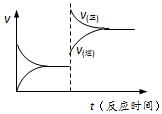
| D. | 反应③达到平衡后升高温度,v(正)、v(逆)的变化如图所示 |
| A. | 0.4mol AgNO3受热完全分解(2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑),用排水法最终收集到气体的分子数为0.2NA | |
| B. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| C. | 1 mol FeI2与一定量氯气反应时,若已知有1mol Fe2+被氧化则转移的电子数为3NA | |
| D. | 1mol 苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
| A. | 113号元素的氧化物为碱性氧化物 | |
| B. | 115号元素位于第七周期VA族 | |
| C. | 含176个中子的Ts原子表示为${\;}_{117}^{176}$Ts | |
| D. | 118号元素的原子最外层有8个电子 |
 25℃时,FeS和ZnS的饱和溶液中,金属阳离子与S2-的物质的量浓度的负对数关系如图所示.下列说法正确的是( )
25℃时,FeS和ZnS的饱和溶液中,金属阳离子与S2-的物质的量浓度的负对数关系如图所示.下列说法正确的是( )| A. | 溶解度S(FeS)<S(ZnS) | |
| B. | a点表示FeS的不饱和溶液,且c(Fe2+)>c(S2-) | |
| C. | 向b点对应溶液中加入Na2S溶液,可转化为c点对应的溶液 | |
| D. | 向c点对应的溶液中加入Na2S溶液,ZnS的KSP增大 |
 在实验室中用浓盐酸与MnO2共热制取Cl2.
在实验室中用浓盐酸与MnO2共热制取Cl2.