题目内容
【题目】某兴趣小组为研究原电池原理,设计如图甲乙两个原电池装置。

(1)如图甲,a和b用导线连接,Cu电极的电极反应式为:________,溶液中SO42-移向______(填“Cu”或“Fe”)极。
(2)如图乙所示的原电池装置中,负极材料是_____。正极上能够观察到的现象是_______________。 负极的电极反应式是_________________。原电池工作一段时间后,若消耗负极5.4g,则放出气体______mol。
(3)将反应Cu + Fe2(SO4)3=2FeSO4 + CuSO4设计成盐桥电池并画图____________

(4)依据Ba(OH)2·8H2O与NH4Cl晶体的反应原理设计原电池,你认为是否可行并说明理由______。
【答案】2H++2e-=H2↑ Fe Al 产生气泡 Al-3e- +4OH-=AlO2- + 2H2O 0.3  否,因为此反应为非氧化还原反应
否,因为此反应为非氧化还原反应
【解析】
(1)甲装置中,a和b用导线连接,该装置构成原电池,铁失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应产生氢气,电解质溶液中阴离子向负极移动,电子由铁电极经导线流向铜电极;
(2)乙装置中,铝与氢氧化钠溶液反应构成原电池,铝失电子发生氧化反应而作负极,镁作正极,正极上氢离子得电子发生还原反应产生氢气;
(3)设计原电池要满足原电池的组成条件;
(4)原电池反应必须是自发进行的放热的氧化还原反应。
(1)甲装置中,a和b用导线连接,该装置构成原电池,铁失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应产生氢气,电极反应式为:2H++2e-=H2↑,电解质溶液中阴离子向负极移动,溶液中SO42-移向铁电极;
(2)乙装置中,铝与氢氧化钠溶液反应构成原电池,铝失电子发生氧化反应而作负极,电极反应式为:Al-3e- +4OH-=AlO2- + 2H2O;镁作正极,正极上氢离子得电子发生还原反应产生氢气,可以观察到产生气泡;由反应总方程式可知:2Al![]() 3H2,5.4g Al的物质的量为
3H2,5.4g Al的物质的量为![]() =0.2mol,则能生成H2的物质的量为0.3mol;
=0.2mol,则能生成H2的物质的量为0.3mol;
(3)将反应Cu + Fe2(SO4)3=2FeSO4 + CuSO4设计成盐桥电池需要Cu作负极,铜电极烧杯中电解质为CuSO4,可用惰性电极作正极,电解质溶液为Fe2(SO4)3溶液,形成闭合回路,装置图为: ;
;
(4)原电池反应必须是自发进行的放热的氧化还原反应,该反应是吸热反应且不是氧化还原反应,所以不能设计成原电池。

【题目】化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空。
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是_____,_________,________,______。

实验编号 | ①中的物质 | ②中的物质 |
1 | 淀粉碘化钾溶液 | 浓硝酸 |
2 | 酚酞溶液 | 浓硫酸 |
3 | 氯化铝溶液 | 浓氨水 |
4 | 湿润的红纸 | 饱和氯水 |
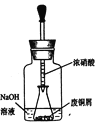
(2)用下图装置:废铜屑制硝酸铜,反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____(填写化学式)。
(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题。
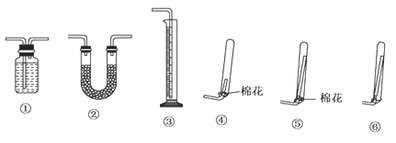
①若要测定生成的NH3的体积,则必须选择的装置是______(填装置序号),装置中所盛试剂应具有的性质是_______,收集干燥的NH3,收集装置应选择(填装置序号)_______,理由是__________。
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1—10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式_______。
(4)下图是苯与溴发生反应并进行产物检验的反应装置:

实验装置中的冷凝管“左低右高”的放置目的是____________,整套实验装置中能防止倒吸的装置是_____(填装置序号)。
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫。
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠。
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠。
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎。
②将研钵中的样品露置在空气中两天。
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡。
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少。
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)________。
(6)如果要验证③是否成立的实验方法是______________________。