题目内容
设NA表示阿伏加德罗常数,下列叙述中正确的是
- A.18gD2O中含有的电子数为10NA
- B.4.6g NO2气体中可能含有0.08NA个NO2分子
- C.29.0g 2CaSO4?H2O晶体中结晶水的数目为0.2NA
- D.在铜与硫的反应中,1mol铜失去的电子数为2NA
B
分析:A、质量换算物质的量,结合质子数计算;
B、质量换算物质的量,结合二氧化氮和四氧化二氮存在化学平衡;
C、质量换算物质的量,结合化学式计算;
D、铜和硫反应生成硫化亚铜.
解答:A、18gD2O物质的量= =0.9mol,含电子数=0.9mol×10=9mol,即9NA,故A错误;
=0.9mol,含电子数=0.9mol×10=9mol,即9NA,故A错误;
B、4.6g NO2气体物质的量为0.1mol,二氧化氮和四氧化二氮存在化学平衡,二氧化氮分子物质的量小于0.1mol,所以4.6g NO2气体中可能含有0.08NA个NO2分子,故B正确;
C、29.0g 2CaSO4?H2O晶体物质的量=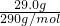 =0.1mol,含结晶水的数目为0.1NA,故C错误;
=0.1mol,含结晶水的数目为0.1NA,故C错误;
D、在铜与硫的反应中,铜和硫反应生成硫化亚铜,1mol铜失去的电子数为NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,注意2CaSO4?H2O化学式的结构分析和摩尔质量的计算,铜与硫反应生成硫化亚铜.
分析:A、质量换算物质的量,结合质子数计算;
B、质量换算物质的量,结合二氧化氮和四氧化二氮存在化学平衡;
C、质量换算物质的量,结合化学式计算;
D、铜和硫反应生成硫化亚铜.
解答:A、18gD2O物质的量=
 =0.9mol,含电子数=0.9mol×10=9mol,即9NA,故A错误;
=0.9mol,含电子数=0.9mol×10=9mol,即9NA,故A错误;B、4.6g NO2气体物质的量为0.1mol,二氧化氮和四氧化二氮存在化学平衡,二氧化氮分子物质的量小于0.1mol,所以4.6g NO2气体中可能含有0.08NA个NO2分子,故B正确;
C、29.0g 2CaSO4?H2O晶体物质的量=
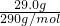 =0.1mol,含结晶水的数目为0.1NA,故C错误;
=0.1mol,含结晶水的数目为0.1NA,故C错误;D、在铜与硫的反应中,铜和硫反应生成硫化亚铜,1mol铜失去的电子数为NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,注意2CaSO4?H2O化学式的结构分析和摩尔质量的计算,铜与硫反应生成硫化亚铜.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目