题目内容
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| B. | 0.1mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 足量的O2与1molNa充分反应,转移的电子数为NA | |
| D. | 50mL12mol•L-1的盐酸与足量MnO2共热,转移电子数为0.3NA |
分析 A、在氢氧化钠溶液中,氢氧根绝大多数来自氢氧化钠的电离;
B、中子数=质量数-质子数;
C、氧气和钠反应后可能变为-2价,也可能变为-1价;
D、二氧化锰只能与浓盐酸,与稀盐酸不反应.
解答 解:A、在氢氧化钠溶液中,氢氧根绝大多数来自氢氧化钠的电离,氢离子全部来自水的电离,而pH=13的NaOH溶液中,氢离子浓度为10-13mol/L,故1L溶液中水电离出的氢离子的物质的量为10-13mol,故水电离出的氢氧根的物质的量也为10-13mol,个数为10-13NA,故A错误;
B、中子数=质量数-质子数,故${\;}_{38}^{90}$Sr原子中中子数=90-38=52,故0.1mol${\;}_{38}^{90}$Sr原子中含有的中子数为5.2NA个,故B错误;
C、钠反应后变为+1价,故1mol钠反应后转移NA个电子,故C正确;
D、二氧化锰只能与浓盐酸,与稀盐酸不反应,故盐酸不能反应完全,则转移的电子数小于0.3NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
12.下列有关实验原理或实验操作正确的是( )
| A. | 利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液 | |
| C. | 用水润湿pH试纸测量某溶液的PH | |
| D. | 实验室用NaOH溶液除去Cl2中的少量HCl |
9.下列说法正确的是( )
| A. | 等质量的铝分别与足量Fe2O3或Fe3O4发生铝热反应时,转移电子的数目相等 | |
| B. | 质量分数分别为40%和60%的硫酸溶液等体积混合,所得溶液的质量分数为50% | |
| C. | 金属钠着火时,立即用泡沫灭火器灭火 | |
| D. | 洗涤做焰色反应的铂丝,可选用稀盐酸或稀硫酸 |
6.下列关于有机物的叙述正确的是( )
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 分子式为C2H6O2且能与NaOH溶液反应的有机物一定是乙酸 | |
| C. | 油脂和纤维素都是能发生水解反应的高分子化合物 | |
| D. | 甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应 |
13.阿伏加德罗常数的值为NA.下列说法正确的是( )
| A. | 1L0.1mol•L-1NH4Cl溶液中,NH4+的数量为0.1NA | |
| B. | 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA | |
| C. | 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA | |
| D. | 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA |
4.电解盐酸和氯化铵的混合溶液,发生反应2H++NH4++3Cl-$\frac{\underline{\;电解\;}}{\;}$3H2↑+NCl3,生成VL气体.设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1mol•L-1的NH4Cl溶液中含NH4+的数目小于0.01NA | |
| B. | 该反应释放H2的分子数为$\frac{V}{22.4}$NA | |
| C. | 反应中每消耗2molH+转移的电子数为6NA | |
| D. | 120.5gNCl3中所含共价键数为4NA |
 3-甲基戊烷
3-甲基戊烷 2,2-二甲基-3-乙基戊烷.
2,2-二甲基-3-乙基戊烷.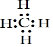 ; B与D组成的三原子分子的结构式为O=C=O.
; B与D组成的三原子分子的结构式为O=C=O.