题目内容
 已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol下列说法中正确的是( )
已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol下列说法中正确的是( )| A、反应过程中能量关系可用如图表示 | B、CH4的燃烧热是820kJ | C、11.2LCH4完全燃烧放出热量410kJ | D、若将此反应设计成原电池,甲烷在正极被氧化 |
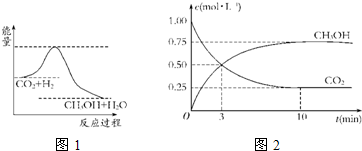
分析:A、反应是放热反应,反应物能量高于生成物;
B、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
C、11.2L甲烷气体,温度压强不是标准状况,物质的量不是0.5mol;
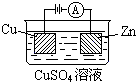
D、设计原电池,燃料在负极失电子被氧化发生氧化反应;
B、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
C、11.2L甲烷气体,温度压强不是标准状况,物质的量不是0.5mol;
D、设计原电池,燃料在负极失电子被氧化发生氧化反应;
解答:解:A、反应是放热反应,反应物能量高于生成物,图象表示能量变化符合反应特征,故A正确;
B、CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol,反应中生成的是气态水,不是我的氧化物,燃烧热大于820kJ/mol,故B错误;
C、11.2L甲烷气体,温度压强不是标准状况,物质的量不是0.5mol,故C错误;
D、若将此反应设计成原电池,甲烷在负极失电子被氧化,故D错误;
故选A.
B、CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol,反应中生成的是气态水,不是我的氧化物,燃烧热大于820kJ/mol,故B错误;
C、11.2L甲烷气体,温度压强不是标准状况,物质的量不是0.5mol,故C错误;
D、若将此反应设计成原电池,甲烷在负极失电子被氧化,故D错误;
故选A.
点评:本题考查了化学反应能量变化的特征分析,燃烧热概念理解,原电池原理的分析应用,掌握基础是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目