题目内容
(1)除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,离子方程式为
(2)除去Fe2+溶液中混入的Fe3+杂质的试剂是 ;离子方程式为 .
(2)除去Fe2+溶液中混入的Fe3+杂质的试剂是
考点:离子方程式的书写,物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:(1)可加入盐酸除杂;
(2)FeCl3可与铁反应生成FeCl2,可加入铁粉除杂.
(2)FeCl3可与铁反应生成FeCl2,可加入铁粉除杂.
解答:
解:(1)因NaCl不能和盐酸反应,NaHCO3能与盐酸反应反应生成氯化钠、水、二氧化碳,生成的氯化钠又溶于水,所以可用盐酸除去混入NaCl溶液中少量NaHCO3杂质,故答案为:盐酸;HCO3-+H+=CO2↑+H2O;
(2)Fe与氯化铁反应生成氯化亚铁,且Fe不能溶于水,选Fe来除杂,发生的离子反应为Fe+2Fe3+═3Fe2+,故答案为:铁粉;Fe+2Fe3+═3Fe2+.
(2)Fe与氯化铁反应生成氯化亚铁,且Fe不能溶于水,选Fe来除杂,发生的离子反应为Fe+2Fe3+═3Fe2+,故答案为:铁粉;Fe+2Fe3+═3Fe2+.
点评:本题考查除杂及离子反应方程式的书写,为高考常见题型,注意除杂的原则及物质的性质即可解答,侧重氧化还原反应的考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
A、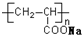 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| B、用于现代建筑的钢筋混凝土不属于复合材料 |
| C、pH=2的盐酸和NH4Cl溶液中,水电离出的c(H+)相等 |
| D、常温时铝遇浓硝酸钝化,是由于铝元素有很强的金属性 |
被蚊虫叮咬后.涂些含有碱性物质(如NH3?H2O)的药水,可减轻痛痒.NH3?H2O中的N元素的化合价为( )
| A、-3 | B、0 | C、+3 | D、+5 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、78g苯分子中含有的碳碳双键数为3NA |
| B、7.8g Na2O2含有的阴离子数目为0.2NA |
| C、12g石墨烯(也就是单层石墨)中含有六元环的个数为NA |
| D、常温常压下,2g D216O中含中子数、质子数、电子数均为NA |
下列离子方程式中正确的是( )
| A、钠和冷水反应 Na+2H2O═Na++2OH-+H2↑ |
| B、Fe片浸泡在FeCl3溶液中:Fe3++Fe═2Fe2+ |
| C、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+═BaSO4↓ |
| D、氯化铝溶液中加入过量的氨水 Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
纪录片《舌尖上的中国》展示了中华饮食文化的博大精深.下列烹饪用品的调味成分不属于有机物的是( )
| A、食盐 | B、香醋 | C、麻油 | D、黄酒 |
将0.015mol Fe3O4完全溶于硫酸中,再加入K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为( )
| A、0.05mol/L |
| B、0.1mol/L |
| C、0.2mol/L |
| D、0.3mol/L |