题目内容
某同学设计如图所示的实验装置来粗略测定电石中碳化钙的质量分数。

(1)烧瓶中发生反应的化学方程式主要是_________________________________。装置B和C的作用是_______________________________________________。烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了____________________________________________________。
(2)所用的电石质量不能太大,否则____________;也不能太小,否则____________。若容器B的容积为250 mL,则所用的电石质量应在____________g左右(从以下数据选填:0.30、0.60、1.00、1.50、2.00)(气体体积以标准状况计)。
(3)实验中测得排入量筒中水的体积为V mL(以标准状况计),电石质量为m g,则电石中碳化钙质量分数是____________(不计算导管中残留的水,气体中饱和水蒸气也忽略不计)。
(1)CaC2+2H2O→Ca(OH)2+C2H2↑ 测量生成气体的体积 防止气体泄漏
(2)实验失败 误差较大 0.60
(3)![]()
解析:
(1)产生的气体进入B,可将B中水排入C,由于V(水)=V(气),所以B、C的作用是测量生成气体的体积。
(2)若电石太大,产生的气体就太多,若V(气)>V(水),则会导致实验失败;若电石太小,产生的气体就太少,就会增大测定误差。V最大(水)=250 mL,n最大(CaC2)=n最小(C2H2)=![]() =0.011 2 mol,m最大(CaC2)=64.0 g·mol-1×0.011 2 mol=0.717 g。由题意,选用电石的质量可为0.60 g。
=0.011 2 mol,m最大(CaC2)=64.0 g·mol-1×0.011 2 mol=0.717 g。由题意,选用电石的质量可为0.60 g。
![]()
m(CaC2)=![]()
![]()

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案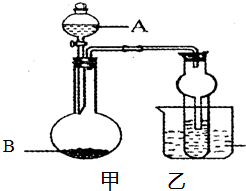 某同学设计如图所示的装置进行实验,请回答:
某同学设计如图所示的装置进行实验,请回答:(1)若试管内盛溴的四氯化碳溶液,液体A跟固体B(电石)在常温下反应,产生的气体可以使溴的四氯化碳溶液褪色,则A可能是
(2)若A为一种酸(HA)溶液,B为碳酸钠固体,试管内盛澄清的苯酚钠溶液,实验过程中观察到试管内溶液变浑浊,再加热烧杯中的水至70℃以上,观察到试管中的现象是
(3)本装置在不加热的条件下除制取乙炔外,还可以进行多种气体的制取和性质实验.请填写编号⑤栏目中的物质的名称或化学式(要求可制得的气体与示例的气体不同,而且设计要合理).
| 编号 | 液体A | 固体B | 可制得的气体 |
| ① | 浓氨水 | NaOH | NH3 |
| ② | 稀硫酸 | Zn | H2 |
| ③ | 稀盐酸 | CaC03 | C02 |
| ④ | 双氧水 | Mn02 | Q |
| ⑤ |
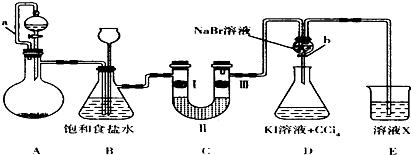
(1)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是(CrCl3),写出A中反应的离子方程式:
(2)拆去a导管的后果可能是
B装置有两个作用,分别是除去氯气中的氯化氢和安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象是
(3)装置c的功能是探究氧化性的物质是否一定有漂白性,下列最佳试剂组合是
| ① | ② | ③ | ④ | |
| I | 湿润的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 湿润的红纸条 |
| II | 碱石灰 | 氯化钙 | 硅胶 | 氯化钠 |
| III | 湿润的红纸条 | 干燥的红纸条 | 干燥的白纸条 | 干燥的红纸条 |
(5)溶液x宜选用下列中的
①氢氧化钠溶液 ②亚硫酸钠溶液 ③亚硫酸氢钠溶液 ④氯化亚铁溶液⑤硫氢化钠溶液 ⑥碳酸氢钠溶液.


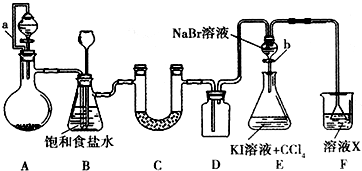 某同学设计如图所示的实验方案,请回答下列问题.
某同学设计如图所示的实验方案,请回答下列问题.