题目内容
氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,下列有关新制氯水的说法中不正确的是( )
| A、新制氯水呈黄绿色,且有刺激性气味,说明氯水中含有Cl2 | B、新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有Cl2 | C、向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明Cl2的氧化性强于I2 | D、新制氯水滴到Na2CO3溶液中,有气体产生,说明氯水中含有H+ |
分析:根据氯气溶于水,部分氯气与水反应发生反应:Cl2+H2O?HCl+HClO,HClO?H++ClO-,HCl=H++Cl-,所以氯水中存在Cl2、H2O、HClO、H+、Cl-、ClO-、OH-,利用离子、分子的性质来分析.
解答:解:A.氯气是黄绿色气体,且有刺激性气味,如果氯水溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在,故A正确;
B.氯气溶于水,部分氯气与水反应发生反应:Cl2+H2O?HCl+HClO,盐酸具有酸性,次氯酸具有漂白性,所以新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有盐酸和次氯酸,故B错误;
C.氯气能氧化碘离子生成单质碘,碘遇淀粉变蓝,向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明Cl2的氧化性强于I2,故C正确;
D.新制氯水中存在盐酸,新制氯水滴到Na2CO3溶液中,发生Na2CO3+2HCl═2NaCl+H2O+CO2↑,有气体产生,说明氯水中含有H+,故D正确;
故选B.
B.氯气溶于水,部分氯气与水反应发生反应:Cl2+H2O?HCl+HClO,盐酸具有酸性,次氯酸具有漂白性,所以新制氯水滴在蓝色石蕊试纸上,试纸先变红色后褪色,可说明氯水中含有盐酸和次氯酸,故B错误;
C.氯气能氧化碘离子生成单质碘,碘遇淀粉变蓝,向淀粉碘化钾溶液中加入氯水,溶液变为蓝色,可证明Cl2的氧化性强于I2,故C正确;
D.新制氯水中存在盐酸,新制氯水滴到Na2CO3溶液中,发生Na2CO3+2HCl═2NaCl+H2O+CO2↑,有气体产生,说明氯水中含有H+,故D正确;
故选B.
点评:本题考查氯水的成分及氯水中各微粒的性质,明确离子、分子的性质是解答本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
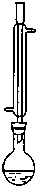 (2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:
(2011?杭州一模)氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行: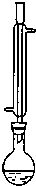 氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行:
氯化苄(C6H5CH2Cl)是一种重要的有机化工原料,广泛应用于医药、染料、助香料等有机化工产品的制备.氯化苄为无色液体,具有强烈的催泪作用,沸点为179.4℃,不溶于水,可混溶于乙醇、氯仿等多数有机溶剂.工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄.为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品进行纯度检测.每一组检测按照如下步骤进行: