题目内容
【题目】A、B、C、D四种强电解质溶液分别含有下列阴、阳离子中的各一种且不重复:NH![]() 、Ba2+、H+、Na+、SO42-、CO32-、NO3-、OH﹣已知:①向A或D中滴入C,均有沉淀生成:
、Ba2+、H+、Na+、SO42-、CO32-、NO3-、OH﹣已知:①向A或D中滴入C,均有沉淀生成:
②向A和B中分别滴加D(可加热)均有气体生成(又已知:D和B反应生成的气体能被A吸收),且这两种气体在水中能反应生成D。 试回答下列问题:
(1)写出A、B、C、D四种溶液中溶质的化学式:
A______________,B______________,C______________,D______________。
(2)将A与D反应生成的气体缓慢通入含KOH、Ca(OH)2、NaAlO2的混合溶液中,生成沉淀的物质的量n与通入气体的体积V的关系可表示______________(填字母)。
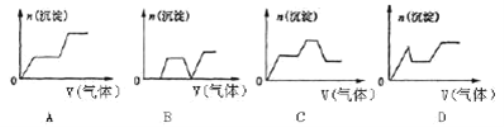
【答案】H2SO4 NaOH Ba(NO3)2 (NH4)2CO3 C
【解析】
(1)解答题目的关键是找到突破口,D和A、B都能生成气体,而题给离子中只有H+与CO32-、OH-与NH4+能反应生成气体,故D只能为(NH4)2CO3;在A或D中滴入C,均有沉淀生成,说明A中含有SO42-,C中应含有Ba2+,而A和D反应生成的气体说明A一定是硫酸,产生的气体是二氧化碳,能被B吸收,说明B是一种碱,所以C是硝酸钡,B是氢氧化钠,以此解答该题;
(2)只要通入CO2,立刻就有沉淀CaCO3产生;将Ca(OH)2消耗完毕,接下来消耗KOH,因而此段不会产生沉淀(即沉淀的量保持不变);KOH被消耗完毕,接下来消耗KAlO2,有Al(OH)3沉淀生成;又因二氧化碳足量,还可以继续与上面反应的产物K2CO3、CaCO3、发生反应。
(1)在NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、CO32-离子中可能生成的气体有NH3和CO2两种,由D和A、B反应生成,则D中含有CO32-和NH4+离子,应为(NH4)2CO3,在A或D中滴入C,均有沉淀生成,说明A中含有SO42-,C中应含有Ba2+,而A和D反应生成气体说明A一定是硫酸,产生的气体是二氧化碳,能被B吸收,说明B是一种碱,所以C是硝酸钡,B是氢氧化钠;
答案为H2SO4、NaOH、Ba(NO3)2、(NH4)2CO3;
(2)通入的CO2先和Ca(OH)2反应生成CaCO3;接着二氧化碳和KOH反应生成K2CO3,二氧化碳和NaAlO2反应生成Al(OH)3;接着和K2CO3反应生成KHCO3;最后二氧化碳和CaCO3反应生成Ca(HCO3)2,符合条件的曲线为选项C。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案【题目】(1)有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和粘合剂等高聚物。为研究X的组成与结构,进行了如下实验:
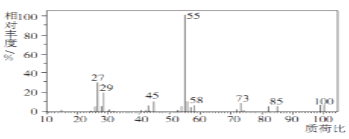
①有机物X的质谱图为:
| 有机物X的相对分子质量是________ |
②将10.0gX在足量O2中充分燃烧,并使其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2g,KOH浓溶液增重22.0g。 | 有机物X的分子式是__________。 |
③经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比是3:1。 | 有机物X的结构简式是______ |
(2)DielsAlder反应为共轭双烯与含有碳碳双键或碳碳三键的化合物相互作用生成六元环状化合物的反应,最简单的反应是:![]() 是由A(C5H6)和B经DielsAlder反应制得。
是由A(C5H6)和B经DielsAlder反应制得。
①DielsAlder反应属于________反应(填反应类型),A的结构简式为________。
②写出与![]() 互为同分异构体,且一溴代物只有两种的芳香烃的名称:________;写出生成这两种一溴代物所需要的反应试剂和反应条件:________,_______
互为同分异构体,且一溴代物只有两种的芳香烃的名称:________;写出生成这两种一溴代物所需要的反应试剂和反应条件:________,_______
【题目】某组甲乙同学进行稀硫酸与锌制取氢气的实验,请回答下列问题:
(1)甲同学发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=___,V6=___,V9=___;
②反应一段时间后,实验A中的金属呈___色,实验E中的金属呈___色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因___________________________。
(2)乙同学为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
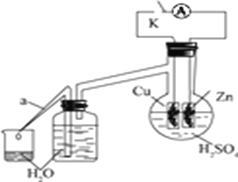
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是__________________________________________________________。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是____________________________________。
【题目】(1)25 ℃时,将体积Va、pH=a的某一元强碱与体积为Vb、pH=b的某二元强酸混合。
①若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=____________。
②为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg![]() 。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,结合H+能力最强的是____。
②根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是__(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3)已知常温下,Ksp[Fe(OH)3]=4.0×10-38,在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:_______;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为__mol/L。