��Ŀ����
��ȡ���� [CO(NH2)2]�ķ�Ӧ��2NH3(g)+CO2(g) 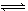 CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
ij�¶������Ϊ10L���ܱ������У���ø����ʵ����ʵ����������£�
|
���ʵ���mol |
0min |
2 min |
3 min |
4 min |
|
NH3 |
2.0 |
1.4 |
n1 |
n1 |
|
CO2 |
1.0 |
0.7 |
n2 |
n2 |
|
H2O |
0 |
0.3 |
n3[ |
n3 |
��1�����ݱ������ݼ���0��2min��NH3��ƽ����Ӧ���� ������ʼʱ��ƽ��ʱ��������ѹǿ֮��Ϊ15/11��n1�� mol��
��2�����¶��´˷�Ӧ��ƽ�ⳣ������ʽΪ
��3�����и����ܱ�ʾ�÷�Ӧ�ﵽƽ��״̬�� ��
A������NH3�����ʵ���������H2O�����ʵ���֮��Ϊ2��1
B��c(NH3)��c(CO2)��c(H2O)=2��1��1
C�������ܶȲ��ٱ仯
D������ѹǿ���ٱ仯
��1��0.03mol/(L��min)��2�֣���1.2��2�֣���2��K�� ��2�֣���3��CD��2�֣�
��2�֣���3��CD��2�֣�
��������
�����������1�����ݱ������ݿ�֪��0��2min��NH3�����ʵ���������2.0mol��1.4mol��0.6mol����Ũ�ȱ仯����0.6mol��10L��0.06mol/L����������ƽ����Ӧ���ʣ�0.06mol/L��2min��0.03mol/(L��min)��
2NH3(g)+CO2(g)  CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
��ʼ����mol�� 2.0 1.0 0
�仯����mol�� ��2.0��n1�� ��1.0��0.5n1�� ��1.0��0.5n1��
ƽ������mol�� n1 0.5 n1 ��1.0��0.5n1��
�����ѹǿ֮������Ӧ��������ʵ���֮�ȿ�֪ ��
��
���n1��1.2
��2����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�ķ���ʽ��֪���÷�Ӧ��ƽ�ⳣ������ʽK�� ��
��
��3����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��A����Ӧ����֮�ȵ�����Ӧ�Ļ�ѧ������֮�ȣ���˸��ݷ���ʽ��֪������NH3�����ʵ���������H2O�����ʵ���֮��ʼ��Ϊ2��1��A����˵����Ӧ�ﵽƽ��״̬��B��ƽ��ʱŨ�Ȳ��ٷ����仯�������ʵ�Ũ��֮�䲻һ����Ȼ�����ij�ֹ�ϵ�����c(NH3)��c(CO2)��c(H2O)��2��1��1����˵����Ӧ�ﵽƽ��״̬��C���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������ݻ�ʼ���Dz���ģ��������Ǽ��ٵģ���˵������ܶȲ��ٱ仯ʱ����˵����Ӧ�ﵽƽ��״̬��D���÷�Ӧ�����������С�Ŀ��淴Ӧ������ѹǿҲ�Ǽ�С�ģ��������ѹǿ���ٱ仯����˵����Ӧ�ﵽƽ��״̬����ѡCD��
���㣺���鷴Ӧ���ʵ��йؼ��㡢ƽ�ⳣ������ʽ��ƽ��״̬���ж�


 ��2013?������һģ���£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��밴Ҫ��ش��������⣺
��2013?������һģ���£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��밴Ҫ��ش��������⣺