题目内容
某温度下,在一个2L的密闭容器中,加人4 mol A和2 molB进行如下反应:3A(g)+2B(g)  4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
| A.此时,B的平衡转化率是40% |
| B.增加B,平衡向右移动,B的平衡转化率增大 |
C.该反应的化学平衡常数表达式是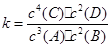 |
| D.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
A
解析试题分析:A、生成1.6 mol C的时候,需要B为0.8 mol,所以B的转化率为40%,正确;B、增加B,平衡向右移动,B的平衡转化率减小,错误;C、因为C是固体,所以不能写在平衡常数关系式中,错误;D、只要温度不变,平衡常数都不变。错误。
考点:考查化学平衡的有关知识。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案在容积为2 L的3个密闭容器中发生反应3A(g)+B(g) xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3 mol A、2 mol B | 6 mol A、4 mol B | 2 mol C |
| 到达平衡的时间(min) | 5 | | 8 |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | | w3 |
| 混合气体密度(g/L) | ρ1 | ρ2 | |
下列说法正确的是( )
A.若x<4,则2c1<c2
B.若w3=w1,可断定x=4
C.无论x的值是多少,均有2ρ1=ρ2
D.容器甲中反应从开始到达平衡平均速率为v(A)=0.3 mol·L-1·min-1
在一恒定的容器中充入2molA和1molB发生反应:2A(g)+ B(g) xC(g),达到平衡后,C的体积分数为ω%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为ω%,则x值为
xC(g),达到平衡后,C的体积分数为ω%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为ω%,则x值为
| A.只能为2 | B.只能为3 |
| C.可能是2,也可能是3 | D.无法确定 |
下列反应在任意温度下一定能自发进行的是( )
A.2NaCl+2H2O 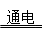 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| B.NH3(g)+HCl(g)=NH4Cl(s) ΔH<0 |
| C.CaCO3(s)=CaO(s)+CO2(g) ΔH>0 |
| D.X2Y2(g)=X2(g)+Y2(g) ΔH<0 |
下列各项不正确的是
| A.等物质的量浓度的下列溶液中① NH4Al(SO4)2② NH4Cl,③CH3COONH4,④ NH3·H2O; c(NH4+),由大到小的顺序是①>②>③>④ |
B.室温下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性 |
| C.25℃时,0.1mol/LCH3COOH溶液V1 mL和0.1mol/L NaOH溶液V2mL混合,若V1>V2,则混合溶液的pH一定小于7 |
D.对于反应 ,在任何温度下都能自发进行 ,在任何温度下都能自发进行 |
在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)  2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
| A.图中a点的值为0.15 |
| B.该反应的平衡常数K=0.03 |
| C.温度升高,平衡常数K值减小 |
| D.平衡时A2的转化率为62.5% |
石墨、金刚石燃烧的热化学方程式分别为:
C(石墨,s)+O2(g) CO2(g) ΔH="-393.51" kJ·mol-1
CO2(g) ΔH="-393.51" kJ·mol-1
C(金刚石,s)+O2(g) CO2(g) ΔH="-395.41" kJ·mol-1
CO2(g) ΔH="-395.41" kJ·mol-1
关于金刚石和石墨的相互转化,下列说法正确的是( )
| A.石墨转化成金刚石是自发进行的过程 |
| B.金刚石转化成石墨是自发进行的过程 |
| C.金刚石比石墨更稳定 |
| D.金刚石比石墨能量低 |
某温度时,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4 mol·L-1,Y2的浓度为0.8 mol·L-1,生成的Z的浓度为0.4 mol·L-1,则该反应的化学方程式(Z用X、Y表示)是( )
A.X2+2Y2 2XY2 2XY2 | B.2X2+Y2 2X2Y 2X2Y |
C.X2+3Y2 2XY3 2XY3 | D.3X2+Y2 2X3Y 2X3Y |
 2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
2C(g),平衡后增大压强,A的百分含量减小,则n≥2。