题目内容
某兴趣小组的同学们共同设计了下图所示的实验装置,此装置即可用于制取气体,又可用于验证物质的某些性质。
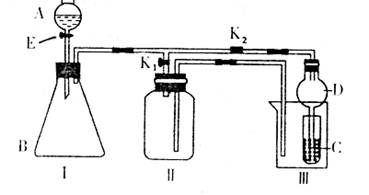
(1)若利用该装置制取并收集H2或NH3,在I中加入药品后应该进行的操作是
;若要制取并收集O2或NO,更换I中药品后,不更换仪器,只需要作简单改进,即可完成实验,其改进的方法是
。
(2)打开K2,关闭K1。
①利用该装置进行实验,可以证明以下物质的酸性强弱顺序为:HC1>H2CO3>H2SiO3。有同学认为:在A中加 ,B中加CaCO3,C中加 (均填写物质的化学式)。观察到 的现象,即可证明。但有的同学认为此实验在证明酸性H2CO3>H2SiO3时有缺陷,你认为缺陷是 。
②利用该装置可以制取C12,并在70℃时与NaOH溶液反应生成NaC1O和NaC1O3。实验方案是:在A中加浓盐酸,B中加高锰酸钾,C中加氢氧化钠溶液,烧杯中加 。待C中溶液恰好反应后,向其中加入过量KI溶液,加入醋酸调节溶液的酸性,此时只有NaC1O被还原,然后用一定浓度的Na2S2O3溶液滴定;继续向其中加入盐酸,调节溶液的酸性,此时NaC1O3被还原,再用同浓度的Na2S2O3溶液滴定。(I2+2S2O32―=S4O62―+2I―)实验结果记录如下:
| 将KI转化为I2 | 滴定I2,消耗Na2S2O3溶液的体积 |
| KI | 5.00mL |
| KI | 30.00mL |
通过表中数据计算C溶液中生成C1O―和C1O3―的物质的量之比 。
(1)关闭K2,打开K1、E 在Ⅱ装置中装满水
(2)①HC1 Na2SiO3 B中固体逐渐溶解,有气体产生,C中有白色胶状沉淀生成 Ⅰ中产生的CO2中混有HC1,通入C中HC1也可与Na2SiO3反应生成H2SiO3沉淀
②70℃的热水或热水 1:2


