题目内容
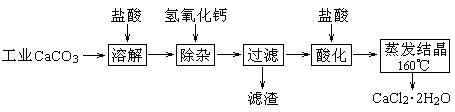
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+、Cu2+等杂质)生产医药级二水合氯化钙(CaCl2?2H2O的质量分数为97.0%~103.0%)的主要流程如下:
![]()
![]()
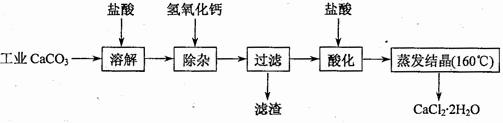
![]() (1)除杂操作是加入氢氧化钙,调节溶液的pH,以除去溶液中的少量Al3+、Fe3+、Cu2+。
(1)除杂操作是加入氢氧化钙,调节溶液的pH,以除去溶液中的少量Al3+、Fe3+、Cu2+。
①已知Cu(OH)2的KSP=2×l0-20 (mol/L)3。要使0. 2mol?L-1CuCl2溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一,此时Al3+、Fe3+已沉淀完全),则应向溶液里加入强碱溶液至溶液的pH为______。
②检验Fe(OH)3已经沉淀完全的实验操作是 ;
③如果将氢氧化钙改为纯净的碳酸钙,请用离子方程式表达除去溶液中Fe3+的过程:
。
![]() (2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其主要目的是: 。
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其主要目的是: 。
![]() (3)测定样品中Cl-含量的方法是:a.称取0.75g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
(3)测定样品中Cl-含量的方法是:a.称取0.75g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用0.05mol?L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
![]() ①上述测定过程中需要溶液润洗的仪器有 。
①上述测定过程中需要溶液润洗的仪器有 。
![]() ②量取25.00mL待测溶液于锥形瓶中时,如果开始滴定管的液面读数为5.10mL,左手控制滴定管的活塞,使待测溶液流入锥形瓶中,眼睛注视着 ,直到 ,迅速关闭活塞。
②量取25.00mL待测溶液于锥形瓶中时,如果开始滴定管的液面读数为5.10mL,左手控制滴定管的活塞,使待测溶液流入锥形瓶中,眼睛注视着 ,直到 ,迅速关闭活塞。
③计算上述所得样品中CaCl2?2H2O的质量分数为 。
![]() ④若用上述办法测定的样品中CaCl2?2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 ; 。
④若用上述办法测定的样品中CaCl2?2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 ; 。
(1)①6(2分)
②取少量上层清液,滴加KSCN溶液,若不出现血红色,则表明Fe(OH)3 沉淀完全。(2分)
③Fe3++3H2OFe(OH)3+3H+ CaCO3+2H+= Ca2++CO2+H2O(2分)
![]() (2)将溶液中的少量Ca(OH)2转化为CaCl2 (2分)
(2)将溶液中的少量Ca(OH)2转化为CaCl2 (2分)
![]() (3)①酸式滴定管
(3)①酸式滴定管![]() (2分)②凹液面的最低处与30.10mL刻度线;液面的最低处与30.10mL刻度线相平(2分)③99.9%
(2分)②凹液面的最低处与30.10mL刻度线;液面的最低处与30.10mL刻度线相平(2分)③99.9%![]() (2分)
(2分)
④样品中存在少量的NaCl(1分) 少量的CaCl2?2H2O失水(1分)




 )测定样品中Cl-含量的方法是:a.称取0.7500 g样品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用0.05000 mol·L-1 AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。
)测定样品中Cl-含量的方法是:a.称取0.7500 g样品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用0.05000 mol·L-1 AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。