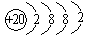题目内容
21g 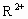 金属离子内含22×3.01×
金属离子内含22×3.01× 个中子,取等质量该元素单质与酸反应生成11.2L氢气(标准状况下).试求:
个中子,取等质量该元素单质与酸反应生成11.2L氢气(标准状况下).试求:
(1)21g 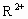 金属离子内含多少摩尔质子,多少摩尔电子?
金属离子内含多少摩尔质子,多少摩尔电子?
(2)R是什么元素?写出该元素原子的核组成符号及原子结构示意图.
答案:
解析:
解析:
|
设该金属为R,则依题意: 又∵21g (0.5mol) ∴1mol (1)21g (2)R是钙元素, |

练习册系列答案
相关题目

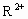 含22×3.01×
含22×3.01×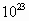 个(11mol)中子,故1mol
个(11mol)中子,故1mol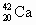 ;Ca
;Ca