题目内容
【题目】配制240mL 1.00mol/L的H2SO4标准溶液的相关操作:①计算;②量取;③稀释、冷却;④转移、洗涤;⑤定容;⑥摇匀。
(1)现用98%的浓硫酸(密度约为1.8g/cm3)来配制,需用量筒量取浓硫酸的体积为_______________。
(2)实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒、_______________、_______________。
(3)下列操作中会引起所配稀硫酸浓度偏大的操作有_______________。(填字母)
A.用量筒量取浓硫酸时,俯视读数
B.从量筒中倒出量取的浓硫酸后洗涤量筒内壁并把洗涤液转入容量瓶中
C.稀释浓硫酸时有少量液体溅出
D.浓硫酸稀释后未冷却就立即转移到容量瓶中 E.容量瓶中残留少量水即用来配溶液
F.定容摇匀后,发现液面低于刻度线
(4)简述上述配溶液时步骤⑤定容时的操作_______________。
【答案】13.9mL 250mL容量瓶 胶头滴管 BD 先将蒸馏水注入容量瓶,当液面距离容量瓶刻度线12cm时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切
【解析】
(1)根据![]() 计算该浓硫酸的物质的量浓度,需要配制240mL1.0mol/L的稀硫酸,但是没有240mL容量瓶,应选择250ml容量瓶,因此实际配制溶液的体积为250mL,再根据稀释定律计算;
计算该浓硫酸的物质的量浓度,需要配制240mL1.0mol/L的稀硫酸,但是没有240mL容量瓶,应选择250ml容量瓶,因此实际配制溶液的体积为250mL,再根据稀释定律计算;
(2)根据配制一定物质的量浓度的溶液的步骤:①计算;②量取;③稀释、冷却;④转移、洗涤;判断实验中所用到的玻璃仪器;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据![]() 进行误差分析;
进行误差分析;
(4)定容时,先将蒸馏水注入容量瓶,当液面距离容量瓶刻度线12cm时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切。
(1)该浓硫酸的质量分数为98%,密度为1.8g/cm3,故该浓硫酸的物质的量浓度![]() ,需要配制240mL 1.0mol/L的稀硫酸,但是没有240mL容量瓶,应选择250ml容量瓶,因此实际配制溶液的体积为250mL,设需要浓硫酸体积为V,根据稀释定律,V×18mol/L=1.0mol/L×0.25L,解得V=13.9mL;
,需要配制240mL 1.0mol/L的稀硫酸,但是没有240mL容量瓶,应选择250ml容量瓶,因此实际配制溶液的体积为250mL,设需要浓硫酸体积为V,根据稀释定律,V×18mol/L=1.0mol/L×0.25L,解得V=13.9mL;
故答案为:13.9mL;
(2)根据配制一定物质的量浓度的溶液的步骤:①计算;②量取;③稀释、冷却;④转移、洗涤;⑤定容;⑥摇匀;判断该实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒、250mL容量瓶、胶头滴管;
故答案为:250mL容量瓶;胶头滴管;
(3)![]() ,如果n偏大或V偏小都导致配制溶液浓度偏大;
,如果n偏大或V偏小都导致配制溶液浓度偏大;
A. 用量筒量取浓硫酸时,俯视读数,导致n偏小,则配制溶液浓度偏小,A项错误;
B. 从量筒中倒出量取的浓硫酸后洗涤量筒内壁并把洗涤液转入容量瓶中,导致n偏大,则配制溶液浓度偏大,B项正确;
C. 稀释浓硫酸时有少量液体溅出,n偏小,则配制溶液浓度偏小,C项错误;
D. 浓硫酸稀释后未冷却就立即转移到容量瓶中并完成定容操作,导致V偏小,则配制溶液浓度偏大,D项正确;
E. 容量瓶中残留少量水即用来配溶液,n、V无影响,则配制溶液浓度无影响,E项错误;
F. 定容摇匀后,发现液面低于刻度线,n、V无影响,配制溶液浓度无影响,F项错误;
故答案为:BD;
(4)定容时,先将蒸馏水注入容量瓶,当液面距离容量瓶刻度线12cm时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切;
故答案为:先将蒸馏水注入容量瓶,当液面距离容量瓶刻度线12cm时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切。

 阅读快车系列答案
阅读快车系列答案【题目】现有氮及其化合物的转化关系如下图,则下列说法错误的是
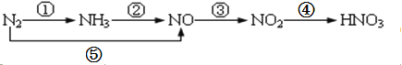
A.路线①②⑤均能表示氮的固定
B.路线②③④是工业生产硝酸的主要途径
C.路线⑤③④是“雷雨发庄稼”的主要途径
D.上述所有反应都是氧化还原反应
【题目】从能量的变化和反应的快慢等角度研究反应具有重要意义。
(1)已知反应2H2(g)+O2(g)=2H2O(g)为放热反应,下图能正确表示该反应中能量变化的是_______ 。
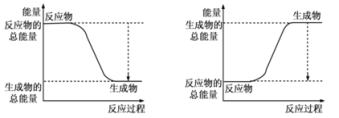
A B
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
从断键和成键的角度分析上述反应中能量的变化。化学键的键能如上表:则生成1mol液态水可以放出热量____________kJ
(2)将质量相同的铜棒和锌棒用导线连接后插入CuSO4溶液中,设计成原电池,负极材料是______________, 正极的反应式为______________,电解质溶液中SO42- 移向______极(填“正”或“负”)。
(3)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为______ ;X为______ 。若反应经2min时C的浓度______ 0.8mol/L(填“大于,小于或等于”)。
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为______ ;X为______ 。若反应经2min时C的浓度______ 0.8mol/L(填“大于,小于或等于”)。