题目内容
17.某有机物的结构如图所示,关于该有机物,下列叙述不正确的是( )
| A. | 该有机物的分子式为C11H12O3 | |
| B. | 能使酸性KMnO4溶液、溴水褪色,原理相同 | |
| C. | 一定条件下,能发生加聚反应又能发生缩聚反应 | |
| D. | 1mol该有机物能与H2发生反应,消耗H24mol |
分析 由结构可知分子式,分子中含碳碳双键、-COOH、-OH,结合烯烃、羧酸、醇的性质来解答.
解答 解:A.由结构可知该有机物的分子式为C11H12O3,故A正确;
B.含碳碳双键与溴水发生加成反应,与高锰酸钾发生氧化反应,褪色原理不同,故B错误;
C.含碳碳双键可发生加聚反应,含-OH、-COOH可发生缩聚反应,故C正确;
D.只有苯环、碳碳双键与氢气发生加成反应,1mol该有机物能与H2发生反应,消耗H24mol,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、羧酸、醇的性质,题目难度不大.

练习册系列答案
相关题目
7.下列各种情况下一定能大量共存的离子组为( )
| A. | Fe3+、Cl-、Na+、SCN- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液中:Al3+、CO32-、Cl-、K+ | |
| C. | 能使甲基橙试剂变黄的溶液:Na+、Cl-、K+、S2O32- | |
| D. | Mg2+、SO42-、I-、Na+ |
8.下列各组离子在溶液中能大量共存的是( )
| A. | Al3+、K+、OH-、NO3- | B. | Ba2+、Na+、SO42-、OH- | ||
| C. | H+、K+、CH3COO-、Cl- | D. | K+、Na+、Cl- |
5.下列说法正确的是( )
| A. | 铁质罐头盒内层镀上一层耐腐蚀的锡,用于防止铁被腐蚀 | |
| B. | 将氯气通入紫色石蕊试液中先变红后褪色,因氯气具有漂白性 | |
| C. | 从海水中提取物质都必须通过化学反应才能实现 | |
| D. | 相同条件下,CuS在CuSO4溶液中的Ksp比在纯水中更小 |
12.下列选项中,有关实验操作、现象和结论都正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将过量的CO2通入CaCl2溶液中 | 无白色沉淀出现 | 生成Ca(HCO3)2可溶于水 |
| B | 过量的Fe粉加入HNO3溶液中,充分反应后,滴入KSCN溶液 | 有气泡产生,溶液变红 | 有氢气生产,稀将Fe氧化为Fe3+ |
| C | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| D | 将SO2通入Ba(NO3)2中 | 有白色沉淀产生 | 有BaSO4沉淀生产 |
| A. | A | B. | B | C. | C | D. | D |
2.下列关于实验基本操作的说法错误的是( )
| A. | 玻璃仪器洗涤干净倒掉水后,水在仪器上应既不能成滴也不能成股流下 | |
| B. | 环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏大 | |
| C. | 将玻璃导管蘸水后,边旋转边向橡皮导管中插入使其连接起来 | |
| D. | 做银镜反应实验后的试管内壁附有银,可用稀硝酸清洗 |
9.当其他条件不变时,下列说法正确的是( )
| A. | 使用催化剂一定能加快反应速率 | |
| B. | 当反应物与生成物浓度相等时,可逆反应一定已达到化学反应限度 | |
| C. | 用粉末状锌代替块状锌与稀硫酸反应一定会加快反应速率 | |
| D. | 在合成氨反应中,增大N2浓度一定可以使H2的转化率达到100% |
1.下列有关过滤和蒸发的操作中,正确的是( )
| A. | 过滤时,漏斗的下端管口紧靠烧杯内壁 | |
| B. | 为了加快过滤速度,可用玻璃棒搅动过滤器中的液体 | |
| C. | 当蒸发皿中的固体完全蒸干后,再停止加热 | |
| D. | 实验完毕后,用手直接取走蒸发皿 |
2.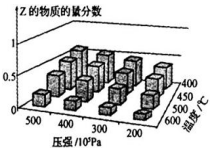 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
( )
 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平 衡时,Z的物质的量分数不变 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0,m+n>c | |
| D. | 温度不变,增大压强,平衡正向移动,达新平衡时,A的浓度比原平衡减小 |