题目内容
下列化学反应方程式正确的是( )
分析:A.铁与盐酸反应生成FeCl2;
B.盐酸酸性强于碳酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳;
C.硝酸+5价氮具有强氧化性,可以将金属氧化到最高价,本身被还原,还原产物与浓度有关,但没有氢气生成;
D.根据铁丝在氧气中点燃生成四氧化三铁进行判断.
B.盐酸酸性强于碳酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳;
C.硝酸+5价氮具有强氧化性,可以将金属氧化到最高价,本身被还原,还原产物与浓度有关,但没有氢气生成;
D.根据铁丝在氧气中点燃生成四氧化三铁进行判断.
解答:解:A.铁与盐酸反应,反应生成的是亚铁,不是三价铁,正确的化学方程式为:Fe+2HCl=FeCl2+H2↑,故A错误;
B.碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,故B错误;
C.硝酸+5价氮具有强氧化性,与金属反应不可能生成氢气,还原产物与浓度有关,如3Zn+8HNO3(稀)=3Zn(NO3)2+2NO↑+4H2O,硝酸很稀时发生4Zn+10HNO3(稀)=4Zn(NO3)2 +NH4NO3+5H2O,故C错误;
D.铁在氧气中燃烧生成四氧化三铁,3Fe+2O2
Fe3O4,故D正确;
故选D.
B.碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,故B错误;
C.硝酸+5价氮具有强氧化性,与金属反应不可能生成氢气,还原产物与浓度有关,如3Zn+8HNO3(稀)=3Zn(NO3)2+2NO↑+4H2O,硝酸很稀时发生4Zn+10HNO3(稀)=4Zn(NO3)2 +NH4NO3+5H2O,故C错误;
D.铁在氧气中燃烧生成四氧化三铁,3Fe+2O2
| ||
故选D.
点评:本题考查化学反应方程式的书写,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号,明确C锌与硝酸的反应原理是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
 用CO合成甲醇(CH3OH)的化学反应方程式为:
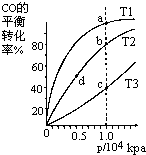
用CO合成甲醇(CH3OH)的化学反应方程式为:CO(g)+2H2(g)?CH3OH(g)△H<0按照相同的物质的量投料,测的CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
| A、平衡常数:K(a)>K(c),K(b)=K(d) | B、正反应速率:v(a)>v(c),v(b)>v(d) | C、平均摩尔质量:M(a)<M(c),M(b)>M(d) | D、平衡时a点一定有n(CO):n(H2)=1:2 |
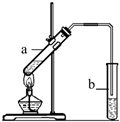 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题: CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O