题目内容
将下列四种化合物分别溶于稀盐酸,滴加硫氰化钾溶液,没有颜色变化,再加氯水即呈现红色的是( )
| A、FeO | B、Fe2O3 | C、FeCl3 | D、Fe2(SO4)3 |
分析:将铁的化合物X溶于盐酸,滴加硫氰化钾溶液不发生颜色变化,则不含三价铁,再加入适量氯水,溶液立即呈红色,说明原物质中含有+2价铁,以此来解答.
解答:解:滴加硫氰化钾溶液没有颜色变化,说明溶液中没有三价铁离子,而三氧化二铁和盐酸反应生成三价铁离子,氯化铁和硫酸铁不与盐酸反应,但溶液中含有铁离子,遇到硫氰化钾溶液会变红,虽然氧化亚铁和稀盐酸反应生成的氯化亚铁溶液中虽然没有铁离子,但加入氯水后,氯水具有很强的氧化性,会把亚铁离子氧化成铁离子,遇硫氰酸钾变红,所以只有FeO符合;
故选A.
故选A.
点评:本题考查了铁及其化合物的有关的化学性质,主要是三价铁离子的检验方法,培养灵活应用知识的能力,题目难度中等.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案
相关题目
 ,阴离子有
,阴离子有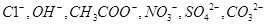 ,现将它们分别配成
,现将它们分别配成 的溶液,进行如下实验:
的溶液,进行如下实验:
 溶液,无明显现象;
溶液,无明显现象;