题目内容
【题目】以![]() 和
和![]() 为原料,通过反应:
为原料,通过反应:![]() 合成尿素。该反应的平衡常数和温度关系如下表;在一定温度和压强下,若原料气中的
合成尿素。该反应的平衡常数和温度关系如下表;在一定温度和压强下,若原料气中的![]() 和
和![]() 物质的量之比
物质的量之比![]() 氨碳比
氨碳比![]() 与
与![]() 平衡转化率
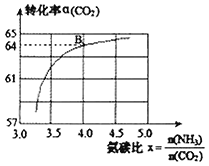
平衡转化率![]() 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
| 165 | 175 | 185 | 195 |
K |
|
|
|
|
A.如图点B处![]() 的平衡转化率为
的平衡转化率为![]()
B.该反应平衡常数的表达式为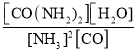
C.该反应中反应物的总键能大于生成物的总键能
D.氨碳比越高,合成![]() 时
时![]() 的转化率越高
的转化率越高
【答案】A
【解析】
A. 设![]() 和
和![]() 物质的量分别为4mol和1mol,
物质的量分别为4mol和1mol,![]() 为
为![]() ,说明
,说明![]() 转化物质的量为
转化物质的量为![]() ,根据方程式,
,根据方程式,![]() 转化物质的量为
转化物质的量为![]() ,
,![]() 的平衡转化率为
的平衡转化率为![]() ,故A正确;
,故A正确;
B. ![]() 和
和![]() 为液态,不在平衡常数的公式中表示,故B错误;
为液态,不在平衡常数的公式中表示,故B错误;
C. 由表格数据可知,随着温度升高,K值变小,说明升高温度,平衡向逆反应方向移动,则该反应是放热反应,反应物的总键能小于生成物的总键能,故C错误;
D. 氨碳比越高,说明氨气的起始物质的量越大,结合转化率![]() ,
,![]() 的转化率减小,故D错误;
的转化率减小,故D错误;
答案选A。

 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】某实验小组研究温度对化学反应![]() 的影响,在其他条件相同时,将
的影响,在其他条件相同时,将![]() 和
和![]() 充入体积为2L的恒容密闭容器中,测得
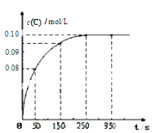
充入体积为2L的恒容密闭容器中,测得![]() 的物质的量分数随时间
的物质的量分数随时间![]() 变化的实验数据如下:
变化的实验数据如下:
时间 | 0 | 20 | 40 | 60 | 80 | 100 | |
|
| 0 |
|
|
|
|
|
| 0 |
|
|
|
|
| |
下列说法正确的是 ![]()
![]()
A. ![]() 温度下,
温度下,![]() 之间,
之间,![]() 的平均反应速率为
的平均反应速率为![]()
B. 在![]() 温度下,该反应有可能在70min时已达到平衡状态
温度下,该反应有可能在70min时已达到平衡状态
C. 由表中数据推测,![]()
D. 由表中数据可知,温度越高,![]() 与
与![]() 的反应限度越大
的反应限度越大
【题目】(1)计算调控值:
室温下,当溶液中c(Mg2+)=c(Cu2+)=0.1mol·L-1时,Mg2+、Cu2+开始沉淀至沉淀完全的pH范围分别为__。已知:Ksp[Mg(OH)2]=10-9、Ksp[Cu(OH)2]=10-15,当c(Mg2+)≤1×10-5mol·L-1时视为沉淀完全。
(2)选择调控值
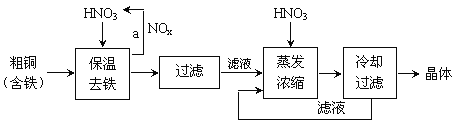
铝灰的回收利用方法很多,现用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下:
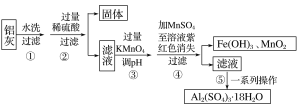
已知步骤③中所得溶液生成氢氧化物沉淀的pH如表所示:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时的pH | 3.4 | 6.3 | 1.5 |
完全沉淀时的pH | 4.7 | 8.3 | 2.8 |
在该浓度下除去铁的化合物,调节pH的最大范围为___。
(3)如何调控
接问题(2),步骤③中调pH时最佳试剂为___。
(4)突破应用
为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀。
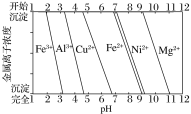
结合题图信息推断该合金中除铜外一定含有__。