题目内容
(思维拓展题)CH2Br-CH2Br可作汽油抗爆剂的添加剂,常温下是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.试管b中装有液溴(表面覆盖少量水).工业用乙烯中常含少量H2S气体.利用工业乙烯通过下列装置可制备少量CH2Br-CH2Br.
填写下列空白.
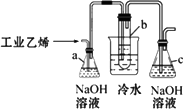
(1)容器a中NaOH溶液的作用是________.
(2)写出本题中制备CH2Br-CH2Br的化学方程式________,该反应属于________反应(填反应类型).
(3)解释将试管b放入盛有冷水的烧杯中的理由:________.
(4)某学生在做此实验时,使用一定量的液溴.当溴全部褪色时,所消耗工业乙烯的量比正常情况下超出许多.试分析其可能的原因________.
答案:
解析:
解析:

解析:本题通过乙烯和溴的加成反应制取1,2-二溴乙烷.
(1)a瓶中的NaOH溶液用于吸收乙烯中的H2S气体,以避免H2S+Br2![]() S↓+2HBr.
S↓+2HBr.
(2)制备1,2-二溴乙烷的方程式为:CH2=CH2+Br2→CH2Br-CH2Br.
此反应为加成反应.
(3)把试管b放入到盛有冷水的烧杯中是为了减少1,2- 二溴乙烷和溴的挥发.
(4)实验过程中消耗工业乙烯的量比正常情况多的原因有两个,一个是装置本身漏气,其二是乙烯通入装置b的速率太快,当乙烯通过试管b时,没有与液溴充分接触反应,而浪费了一部分乙烯.

练习册系列答案
相关题目
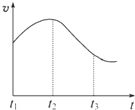 (思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
(思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验: