题目内容
【题目】将一定量的铁粉投入FeCl3溶液中,两者恰好完全反应,完成下列问题。
(1)写出该反应的离子方程式并标出电子转移的方向和数目__________________。
(2)该反应中氧化产物和还原产物的物质的量之比为____________。
(3)若反应过程中转移了0.2mol电子,则溶解消耗的铁的质量为___________。
(4)如何检验某未知溶液中是否含有Fe3+________________________
【答案】 1:2 5.6g 取少量未知液于试管中,向其中滴加少量的KSCN溶液,振荡、观察,若溶液变红,则说明未知液中存在Fe3+;若溶液不变红,则说明原溶液中不存在Fe3+
1:2 5.6g 取少量未知液于试管中,向其中滴加少量的KSCN溶液,振荡、观察,若溶液变红,则说明未知液中存在Fe3+;若溶液不变红,则说明原溶液中不存在Fe3+
【解析】
铁粉投入FeCl3溶液中,反应生成氯化亚铁;该反应中氧化产物和还原产物都为Fe2+,根据氧化还原反应分析氧化产物和还原产物的物质的量;根据反应方程式,1mol铁反应转移2mol电子;检验某未知溶液中是否含有Fe3+常用KSCN溶液。
(1)铁粉投入FeCl3溶液中,反应生成氯化亚铁,因此该反应的离子方程式Fe+2Fe3+=3Fe2+,
标出电子转移的方向和数目 ;故答案为:
;故答案为: 。
。
(2)该反应中氧化产物和还原产物都为Fe2+;还原剂有1mol,氧化产物是化合价升高得到的产物,因此氧化产物有1mol,氧化剂有2mol,还原产物是化合价降低得到的产物,因此还原产物有2mol,氧化产物和还原产物的物质的量之比为1:2;故答案为:1:2。
(3)根据反应方程式,1mol铁反应转移2mol电子,若反应过程中转移了0.2mol电子,则溶解消耗的铁的物质的量为0.1mol,消耗铁的质量为0.1mol×56 gmol1=5.6g;故答案为:5.6g。
(4)检验某未知溶液中是否含有Fe3+的方法是:取少量未知液于试管中,向其中滴加少量的KSCN溶液,振荡、观察,若溶液变红,则说明未知液中存在Fe3+;若溶液不变红,则说明原溶液中不存在Fe3+;故答案为:取少量未知液于试管中,向其中滴加少量的KSCN溶液,振荡、观察,若溶液变红,则说明未知液中存在Fe3+;若溶液不变红,则说明原溶液中不存在Fe3+。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案【题目】新冠肺炎疫情期间,多种含氯消毒剂如84消毒液、Cl2、NaClO2等对病毒均具有很好的消杀作用,其中亚氯酸钠(NaClO2)在工业上常以ClO2气体为原料制备,实验室制备亚氯酸钠的装置如图所示(夹持装置已略)。
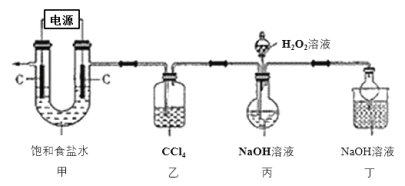
已知:①控制电压电解饱和食盐水可得到ClO2;
②Cl2易溶于CCl4;
③亚氯酸钠在不同温度下的溶解度如下表所示:
温度℃ | 20 | 40 | 60 |
溶解度/g | 6.2 | 23.4 | 48.3 |
回答下列问题:
(1)装置甲中产生ClO2的电极反应式为_____________________。
(2)装置乙中CCl4的作用为________________________________。
(3)装置丙中生成NaClO2的化学方程式为____________________________。
(4)从装置丙反应后的溶液中获得NaClO2晶体的步骤如下:
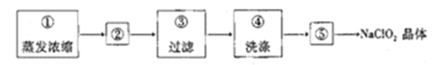
其中步骤①加热到_________________(填现象)时停止加热,步骤②是__________________。
(5)准确称取2.26gNaClO2粗品,加入盛有20.00mL刚煮沸并冷却过的水、足量10%的稀硫酸和30.00mL质量分数为40%的KI溶液(足量)的碘量瓶中,立即密封并摇晃碘量瓶至试样完全反应,再加入淀粉作指示剂用浓度为3.00mol/L的Na2S2O3溶液滴定(已知整个过程中发生的反应依次为![]() +4I-+4H+=2I2+Cl-+2H2O,
+4I-+4H+=2I2+Cl-+2H2O,![]() ),
),
①若三次平行实验测得消耗的Na2S2O3溶液的平均体积为30.00mL,则粗品的纯度为_________________%(保留三位有效数字),
②若使用的水未煮沸,则测定结果会___________________(填“偏高”“偏低”或“无影响”)。