题目内容
9.镍具有优良的物理和化学特性,是高技术产业的重要材料,羰基法提纯粗粗镍涉及的反应为Ni(s)+4CO(g)$\stackrel{50℃}{?}$Ni(CO)4(g).已知该反应的平衡常数K随温度T的变化如下表所示:| T/℃ | 25 | 80 | 230 |
| K | 5×104 | 1 | 2×10-5 |
(1)升高温度,Ni的转化率减小(填“增大”“减小”或“不变”).
(2)在保持温度不变的情况下,要提高上述反应中Ni的转化率,可采取的一种措施是增大压强或降低温度或增加一氧化碳的浓度.
分析 图表的反应平衡常数随温度升高减小,说明升温平衡逆向进行,正反应为放热反应,
(1)反应是放热反应,升温平衡逆向进行,Ni的转化率减小;
(2)要提高上述反应中Ni的转化率,应使平衡正向进行,结合影响化学平衡的因素分析判断.
解答 解:图表的反应平衡常数随温度升高减小,说明升温平衡逆向进行,正反应为放热反应,
(1)Ni(s)+4CO(g)$\stackrel{50℃}{?}$Ni(CO)4(g).反应是放热反应,升温平衡逆向进行,Ni的转化率减小,故答案为:减小;
(2)要提高上述反应中Ni的转化率,应使平衡正向进行,反应是气体体积减小的放热反应,可以增大压强、降低温度、增加一氧化碳的浓度等措施,
故答案为:增大压强或降低温度或增加一氧化碳的浓度.
点评 本题考查了影响化学平衡的因素分析,平衡常数随温度变化判断反应能量变化,平衡移动原理和反应特征分析是解题关键,题目较简单.

练习册系列答案
相关题目
19.意大利科学家最近合成了一种新型的氧分子,其化学式为O4.下列关于O4说法正确的是( )
| A. | 一分子O4由两分子O2构成 | |
| B. | O4是一种单质 | |
| C. | 等质量的O4和O2含有相同数目的分子 | |
| D. | O4是一种化合物 |
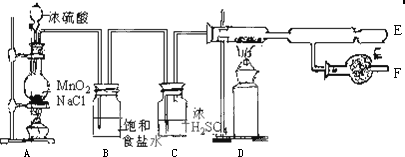
5. 实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
(1)a装置的名称是滴液漏斗(分液漏斗),B中安装导管b 的作用是防止D发生堵塞时出现危险(平衡装置内气压),在加热A过程中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是b;(填正确选项前的字母)
a.引发反应 b.减少副产物乙醚生成 c.防止乙醇挥发
(2)在装置C中应加入氢氧化钠溶液,其目的是吸收反应中可能生成的酸性气体SO2和CO2.
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、下“);
(4)若产物中溶有少量副产物乙醚,可用蒸馏的方法除去;
(5)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是温度太低,1,2-二溴乙烷容易凝固发生堵塞,不安全.
 实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:(1)a装置的名称是滴液漏斗(分液漏斗),B中安装导管b 的作用是防止D发生堵塞时出现危险(平衡装置内气压),在加热A过程中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是b;(填正确选项前的字母)
a.引发反应 b.减少副产物乙醚生成 c.防止乙醇挥发
(2)在装置C中应加入氢氧化钠溶液,其目的是吸收反应中可能生成的酸性气体SO2和CO2.
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、下“);
(4)若产物中溶有少量副产物乙醚,可用蒸馏的方法除去;
(5)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是温度太低,1,2-二溴乙烷容易凝固发生堵塞,不安全.
| 本题中出现有机物相关数据 | |||
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
9.将3mol A与3mol B混合于3L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+nD(g),2s后达平衡A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断正确的是( )
| A. | v(B)=0.25 mol•L-1•s-1 | B. | C的体积分数为30% | ||
| C. | B的转化率为25% | D. | n=2 |
10.下列离子方程式中,正确的是( )
| A. | 铁粉与氯化铁溶液混合:Fe+Fe3+=2Fe2+ | |
| B. | 氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O |
 ;
; 的系统命名为3-甲基戊烷;
的系统命名为3-甲基戊烷;