题目内容
17.判断题1.HCl和HBr有还原性而HI无还原性错
2.碘单质和碘离子的特性是遇淀粉溶液变蓝色错
3.溴、碘在CCl4中的溶解度比在水中的溶解度大得多对
4.AgCl、AgBr、AgI均有感光性,且都是难溶于水的白色物质错.
分析 1、HCl和HBr、HI均有还原性;
2.碘单质遇淀粉溶液变蓝色;
3.溴、碘易溶于CCl4;
4.AgBr有感光性,AgCl、AgBr、AgI都是难溶于水的有色物质.
解答 解:1、HCl和HBr、HI均有还原性;故答案为:错;
2.碘单质遇淀粉溶液变蓝色,但是碘离子不能,故答案为:错;
3.溴、碘易溶于CCl4,在CCl4中的溶解度比在水中的溶解度大得多,故答案为:错;
4.AgAgBr有感光性,三者都是难溶于水的有色物质,AgCl是白色、AgBr浅黄色、AgI黄色,故答案为:错.
点评 本题考查学生卤素离子的还原性、单质的物理性质以及卤化银的溶解情况等,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
5.某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-?H++A2-.现有体积各为10mL的下列四种溶液:
①0.02mol•L-1的H2A溶液
②0.02mol•L-1的NaHA溶液
③浓度均为0.02mol•L-1的Na2A溶液和NaHA的混合溶液
④0.02mol•L-1的Na2A溶液
下列关于上述四种溶液的说法不正确的是( )
①0.02mol•L-1的H2A溶液
②0.02mol•L-1的NaHA溶液
③浓度均为0.02mol•L-1的Na2A溶液和NaHA的混合溶液
④0.02mol•L-1的Na2A溶液
下列关于上述四种溶液的说法不正确的是( )
| A. | 在②的溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+) | |
| B. | 四种溶液中离子总数的关系:④>③>②>① | |
| C. | 四种溶液中c(H+)的关系:①>②>③>④ | |
| D. | 在①的溶液中:c(H+)=c(HA-)+c(A2-)+c(OH-) |
2.锂电池以锂离子非水溶剂为电解质,锂为负极,Li2FeS2为正极.电池反应为2Li+FeS2═Li2FeS2.下列推断正确的是( )
| A. | 放电时.将电能转化成化学能 | |
| B. | 充电时,阳极反应为Li++e-═Li | |
| C. | 正极的电极反应式为FeS2+2e-+2Li+═Li2FeS2 | |
| D. | 每转移0.1mol电子,正极材料消耗12.0g |
17.在2L密闭容器中进行反应:mX(g)+nY(g)?pZ(g)+qQ(g),式中m、n、p、q为化学计量数.在0~3min内,各物质物质的量的变化如下表所示:
已知2min内v(Q)=0.075mol/(L•min),v(Z):v(Y)=1:2
(1)试确定以下物质的相关量:起始时n(Y)=2.3mol,平衡常数K=0.3(保留一位有效数字).
(2)写出反应的化学方程式X(g)+4Y(g)?2Z(g)+3Q(g).
(3)用Z表示2min内的反应速率0.05mol/(L.min).
(4)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-218.0kJ/mol.
| 物质 时间 | X | Y | Z | Q |
| 起始/mol | 0.7 | 1 | ||
| 2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| 3min末/mol | 0.8 |
(1)试确定以下物质的相关量:起始时n(Y)=2.3mol,平衡常数K=0.3(保留一位有效数字).
(2)写出反应的化学方程式X(g)+4Y(g)?2Z(g)+3Q(g).
(3)用Z表示2min内的反应速率0.05mol/(L.min).
(4)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-218.0kJ/mol.
18.某无色溶液,其中可能存在的离子有:Na+、Ag+、Ba2+、Fe3+、Al3+、AlO2-、S2-、SO32-、CO32-、SO42-,现取该溶液进行实验,实验结果如下:
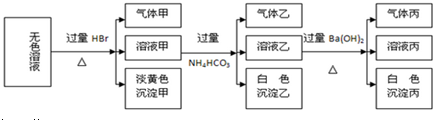
试回答下列问题:
(1)生成沉淀甲的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O.
(2)由溶液甲生成沉淀乙的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入如表(表中每一行对应正确即可得分)
(4)综上所述,该溶液肯定存在的离子有:AlO2-、S2-、SO32-、CO32-、Na+.
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是取沉淀丙加入足量的稀盐酸,若沉淀不完全溶解,则原溶液中含有SO42-;若沉淀完全溶解,则没有SO42-.

试回答下列问题:
(1)生成沉淀甲的离子方程式为:2S2-+SO32-+6H+=3S↓+3H2O.
(2)由溶液甲生成沉淀乙的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(3)已知气体甲由两种氧化物组成(不包括水蒸汽和HBr),请你设计实验逐一鉴别这两种成分,将所需试剂以及现象填入如表(表中每一行对应正确即可得分)
| 步骤 | 实验目的 | 试剂 | 现象 |
| 1 | |||
| 2 | |||
| 3 | 检验CO2 | 澄清石灰水 | 溶液变浑浊 |
(5)针对溶液中可能存在的离子,用实验证明是否存在的方法是取沉淀丙加入足量的稀盐酸,若沉淀不完全溶解,则原溶液中含有SO42-;若沉淀完全溶解,则没有SO42-.
 .
.